- Determination of Site-specific Denitrification Rate for Nitrate Reactive Transport Modeling in Groundwater
Sang Hyun Kim1·Jaeshik Chung1,2*·Seunghak Lee1,2,3*
1Water Cycle Research Center, Korea Institute of Science and Technology (KIST), Seoul 02792, Republic of Korea
2Division of Energy and Environmental Technology, KIST School, Korea University of Science and Technology (UST), Seoul 02792, Republic of Korea
3Graduate School of Energy and Environment (KU-KIST Green School), Seoul 20841, Republic of Korea- 지하수 내 질산성 질소 반응-이동 모델링을 위한 부지특이적 탈질화 계수 선정 방안에 대한 고찰
김상현1·정재식1,2*·이승학1,2,3*
1한국과학기술연구원 물자원순환연구단
2과학기술연합대학원대학교(UST) 에너지-환경융합전공
3고려대학교 에너지환경대학원This article is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
A simple and efficient scheme is presented that attempts to implement the site-specific denitrification rate in the reactive transport modeling for the nitrate in groundwater. A series of correlation analyses were conducted using 133 datasets obtained from different nitrate-contaminated sites to find the empirical relationships between denitrification rates and various subsurface properties. Based on Pearson’s correlation analysis, the soil organic carbon concentrations showed a statistically significant correlation (r = 0.75, p < 0.05) with the denitrification rates. A linear regression was performed, which could be utilized to effectively determine the site-specific denitrification rate based on the soil organic carbon concentration of a site. The proposed method is expected to effectively replace the conventional methods which either were too complicated for practical application or impose large uncertainties that might end up with unreliable results.
Keywords: Groundwater; nitrate; reactive-transport modeling; site-specific denitrification rate; soil organic carbon
지하수의 질산성 질소 오염은 주로 비료, 가축 분뇨와 같은 비점오염원에 의해 발생하며, 전세계적으로 심각한 환경문제로 인식되고 있다(Burri et al., 2019; Re et al., 2017). 토양지하수정보시스템(2021)에 따르면 우리나라에서도 지하수를 음용하는 일부 지역에서 지하수 내 질산성 질소의 농도가 먹는물수질기준(10 mg∙L-1; (환경부, 2021))을 초과하는 사례가 빈번히 보고되고 있다. 일정 농도 이상의 질산성 질소를 장기간 섭취할 경우 내분비계에 교란을 주는 등(Poulsen et al., 2018) 인체에 독성을 유발할 수 있어 지하수 내 질산성 질소 오염 평가 및 관리의 중요성은 보건환경 측면에서도 매우 높다고 할 수 있다(Koh et al., 2020). 질산성 질소는 토양입자에 쉽게 흡착되지 않고 이동성이 큰 특징이 있기 때문에(Birkinshaw and Ewen, 2000; Meisinger and Randall, 1991; Shamrukh et al., 2001), 지하수의 질산성 질소 오염을 효율적으로 평가하고 관리하기 위해서는 특정 시점·위치에서의 농도측정뿐 아니라, 오염 확산을 예측할 수 있는 반응-이동 모델링이 수반되어야 한다.
환원 조건의 지중환경에서 질산염(NO3-)은 이산화질소(NO2-), 일산화질소(NO), 아산화질소(N2O) 등을 거쳐 최종적으로 질소가스(N2)로 변환되는 탈질 반응을 겪을 수 있다(Tilstra et al., 2019). 탈질 반응은 미생물을 매개로 일어나는 생물학적(biotic) 반응과 광물 등이 매개한 비생물학적(abiotic) 반응으로 구분할 수 있는데, 생물학적 탈질 반응의 속도가 상대적으로 더 빠르다고 알려져 있다(Jeon et al., 2020). 지하수 내 질산성 질소 농도는 이와 같은 탈질 반응에 의해 자연적으로 감소될 수 있으며, 따라서 지하수 내 질산성 질소의 반응-이동 모델링 시 이송(advection)이나 확산(dispersion) 이외에도, 탈질 반응에 의한 농도저감이 적절히 반영되어야 한다. 이와 관련한 최근 연구에서(Karanasios et al., 2010; Chung et al., 2019; Lin and Gu, 2020), 질산성 질소의 탈질은, 시·공간에 따른 탈질 속도 변화를 반영하기 위해, 반응에 관여하는 질소 부산물(NO2-, N2,), 전자공여체인 유기물 및 기타 수질인자들을 정량하고, 이에 화학반응속도식(reaction kinetics)을 적용하여 해석하는 방법이 사용되어왔다. 이에 반해, 현장조건을 근거로 산정된 탈질화 계수(denitrification rate)를 대상 영역 전반에 걸쳐 적용하는 약식 모델링 기법도 적용된 바 있는데(Huan et al., 2020; Koh et al., 2018; Wei et al., 2019), 이 경우, 반응-이동 모델에 관여하는 다양한 변수의 불확실성을 고려해야 하는 상황에서 필요한 연산량을 효과적으로 줄일 수 있을 뿐 아니라, 일정한 수준의 정확도를 나타내는 것으로 보고되었다. 특히, 현장 특성치를 미지수로 두고 제한된 수의 관측값을 활용해 수행하는 역산 모델링(inverse modeling)의 경우, 탈질화 계수를 선정하여 모델링하는 방식이 훨씬 효과적일 수 있다. 하지만, 이러한 약식 반응-이동 모델링을 적용할 경우, 신뢰성 있는 모델링 결과를 도출하기 위해서는 대상 지역의 탈질 특성을 적절히 반영한 탈질화 계수 선정이 필수적이다. 하지만, 상당수의 기존 문헌들(Almasri and Kaluarachchi, 2007; Bonton et al., 2011; Chowdary et al., 2004)은 모델링 대상 지역의 수리지질학적 특성, 오염원의 위치 및 규모 등, 모델링 도메인 구성과 관련된 수리지질학적 인자들에 초점을 맞추어 모델링을 진행해 왔으며, 상대적으로 탈질화 계수의 영향에 대해서는 중요하게 다루지 않거나, 심지어 질산성 질소를 비반응성 물질로 간주해 모델에 적용한 사례도 보고된 바 있다(Gupta et al., 2020).
이에 본 연구에서는 대수층에서의 질산성 질소 반응-이동 모델링 시 적절한 탈질화 계수를 선정할 수 있는 방안을 마련하고 제안하였다. 먼저, 기존 문헌들에서 질산성 질소의 탈질화 계수를 선정한 방법을 정리하고 그 한계 및 잠재적 문제를 파악하였다. 이후, 현장 연구 기반의 다양한 문헌들을 분석하여, 탈질 반응과 관련된 부지특성치를 선별하고, 각 특성치와 현장에서 관찰된 탈질화 효율의 상관관계를 파악함으로써, 부지특이적인 탈질화 계수 선정 방안을 도출하였다.
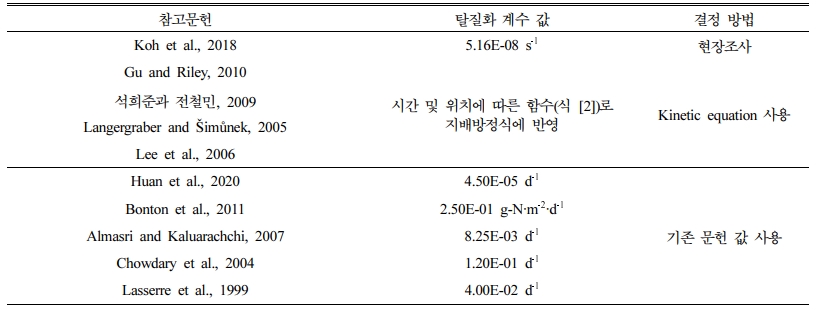
질산성 질소 모델링 관련 기존 연구들에서 탈질화 계수를 결정한 방법을 조사하여 Table 1에 정리하였다. 탈질화 계수 결정 방법은 크게, 1) 현장조사 및 실험, 2) 화학반응속도론에 근거한 계산, 그리고 3) 대푯값 적용으로 구분할 수 있었으며, 각 방법의 특징과 그에 따른 한계점을 Table 1에 서술하였다.
2.1. 현장조사 및 실험을 통한 탈질화 계수 결정방법
Koh et al.(2018)은 제주도 지역에서 지하수 질산성 질소 모델링 연구를 수행하였는데, 모델링 과정에 필요한 탈질화 계수를, 같은 지역에서 수행한 현장조사 결과(Koh et al., 2012; Koh et al., 2016)를 활용하여 결정하였다. 이들은 제주도 고산 지역에 21개 지하수 관정을 설치하여 2009년 2월부터 2010년 10월까지 지하수 내 질산성 질소 농도 및 질소, 산소의 동위원소 조성비(δ15N, δ18O)를 관찰하였다. 이러한 장기간의 현장 조사 결과와, 탈질 반응이 일어날 경우 질산성 질소 농도가 감소하고 δ15N 및 δ18O가 증가한다는 이전 연구 결과(Böttcher et al., 1990)를 바탕으로 대상 지역 지하수에서 탈질화가 진행되고 있음을 확인하였으며, 현장조사를 통해 시간에 따른 질산성 질소 농도 변화를 관찰하여 탈질화 계수를 5.16E-08 s-1로 결정하였다. 이와 같이 모델링 대상 지역에서 현장조사 및 실험을 수행하는 경우 부지특이적 탈질화 계수를 직접적인 방법으로 획득하여 모델링에 사용할 수 있으나, 관측정 설치가 필요하고, 장기간 모니터링 과정이 요구된다는 현실적인 어려움 때문에 이러한 방법을 사용한 기존 연구는 극히 제한적으로 보고되고 있다.
2.2. 화학반응속도론(reaction kinetics)에 근거한 탈질화 계수 결정방법
또 다른 방법은 식 (1)과 같이 전자공여체를 비롯해 탈질 반응에 관여하는 모든 화학종의 농도를 측정한 뒤, 식 (2)와 같은 반응속도 계산식(rate expression)을 이용하여 탈질화 계수를 결정하는 방법이다(Gu and Riley, 2010; Langergraber and imùnek, 2005; Lee et al., 2006; 석희준과 전철민, 2009).

여기서, r은 특정 환경에서의 탈질화 계수(M∙L-3∙T-1), μmax는 최대 탈질화 속도(T-1), Xb는 미생물의 biomass 농도(M∙L-3), kb는 미생물 biomass 관련 상수(M∙L-3), kINO2는 산소에 의한 inhibition 관련 상수(M∙L-3)이며, KCH2O 및 KNO3는 각각 CH2O 및 NO3에 대한 포화상수(M∙L-3)이다. 모델링 대상지역의 용존 산소([O2]), 용존 유기물([CH2O]), 질산성 질소([NO3-]) 농도를 식 [2]에 대입함으로써 탈질화 계수를 산정할 수 있는데, 이러한 반응속도 계산식은 일반적으로 하나의 탈질화 계수 값을 산정하여 수치모델에 전반적으로 사용하기 보다는, 차분화된 시간 및 위치에 따라 서로 다른 값을 적용한다. 이러한 방법은 모델링 대상지역의 용존 산소, 유기물, 질산성 질소 농도 등의 현장 특성을 반영할 수 있고, 시간 및 위치에 따른 탈질화 계수 값의 변화를 모델링에 반영할 수 있다는 장점이 있으나, 다양한 가정을 바탕으로 제한된 조건에서 도출된 식을 사용하는 만큼 불확실성이 존재하며(예를 들어, 전자공여체로 사용된 유기탄소의 종류에 따라 식(1)의 계수들이 달라질 수 있음), 무엇보다 복잡한 화학반응식을 차분화된 시∙공간에 적용하는데 있어 고도화된 연산장치와 수치해석적 배경지식을 요구한다는 단점이 있다(Clement, 1999; Xu et al., 2011).
2.3. 대푯값으로 탈질화 계수를 결정하는 방법
세 번째는 다수의 문헌들(Almasri and Kaluarachchi, 2007; Bonton et al., 2011; Chowdary et al., 2004; Huan et al., 2020; Lasserre et al., 1999)에서 확인할 수 있듯이, 기존 문헌들에 제시된 탈질화 계수 대푯값을 그대로 사용하는 방법이다. 가장 간단한 방법이지만 모델링 대상 지역의 특성을 명확히 반영할 수 없으며, 결과에 큰 불확실성을 포함할 수 있다는 우려가 있다. 실제로 Almasri and Kaluarachchi(2007)의 연구에서 탈질화 계수 값으로 기존 문헌(Frind et al., 1990)에 제시된 8.25E-03 d-1를 사용한 결과, 질산성 질소 모델링 결과값과 실제 관측값 사이에 상당한 오차(약 ±30% 이상)가 발생하는 것을 확인하였다.
앞서 서술한 바와 같이, 기존 연구들에서 사용된 세 가지 탈질화 계수 결정 방법들에는 서로 다른 한계점이 존재하며, 이는 결국 질산성 질소 모델링 결과에 큰 오류를 초래할 수 있다. 이를 보완하기 위해서는 모델링 대상 지역에 적합한 부지특이적 탈질화 계수를 효과적으로 선정할 수 있는 방안 마련이 필요하다.
3.1. 현장 연구 문헌 조사를 통한 탈질화 계수 데이터베이스화
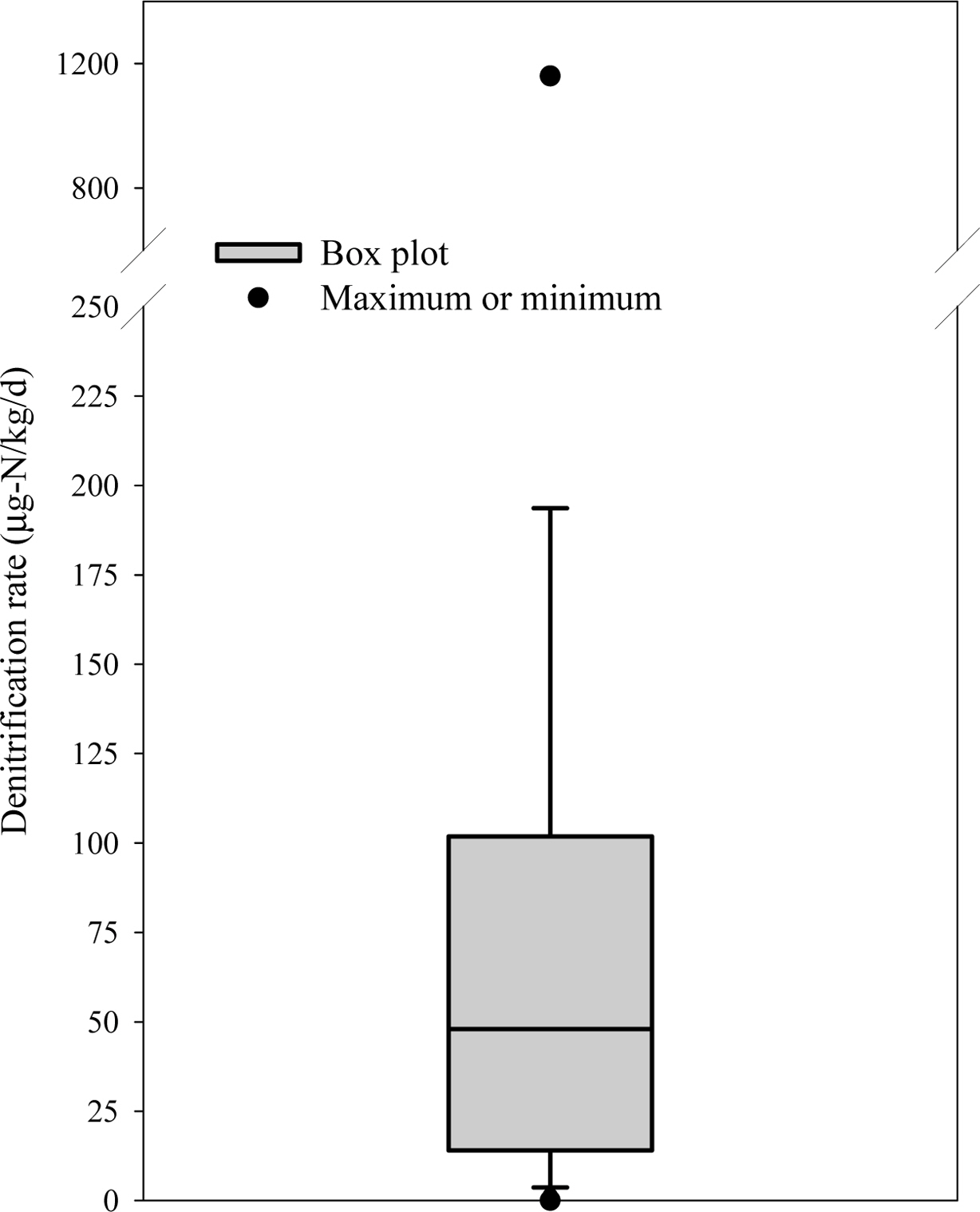
우선, 기존 문헌들에 보고된 다양한 탈질화 계수 값들을 조사하였다. 현장 포화대 영역을 조사하여 N2, N2O 등 탈질 반응 생성물 농도를 직접 측정함으로써 탈질화 계수를 결정한 문헌, 또는 포화대 영역에 존재하는 토양 및 sediment를 샘플링하여 실내실험을 통해 탈질화 계수를 결정한 문헌 등 현장조사 및 실험 기반 문헌들(Bradley et al., 1992; Dhakal et al., 2013; Francis et al., 1989; Hansen, 1989; Harrison et al., 2011; Jahangir et al., 2013; Lind, 1983; Morris et al., 1988; Senko et al., 2005; Van Rijn et al., 1996; Well et al., 2003)을 참고하여 총 138개 탈질화 계수 데이터를 수집하였다. 이 중 5개의 데이터만이 1차 반응상수의 단위(h-1)로 제시되었으며, 1.7E-10–4.9E-07 h-1의 범위를 보였다. 그 외 133개 데이터는 모두 0차 반응상수 단위(μg-N∙kg-1∙d-1)로 제시되었는데(Fig. 1), 0.0–1,160.0 μg-N∙kg-1∙d-1의 넓은 범위를 보였으며, 평균과 표준편차는 각각 98.9, 170.2 μg-N∙ kg-1∙d-1로 나타났다. 이처럼 탈질화 계수는 현장 특성에 따라 다양하게 변화할 수 있는 것으로 확인되었으며, 평균값과 같은 단순한 통계치를 대푯값으로 제시할 경우 큰 불확실성이 포함될 것으로 판단된다. 즉, 적절한 탈질화 계수 값을 선정하기 위해서는 현장 특성이 고려된 계수의 선별이 필요할 것으로 사료된다.
3.2. 지중환경 특성치와 탈질화 계수의 상관관계
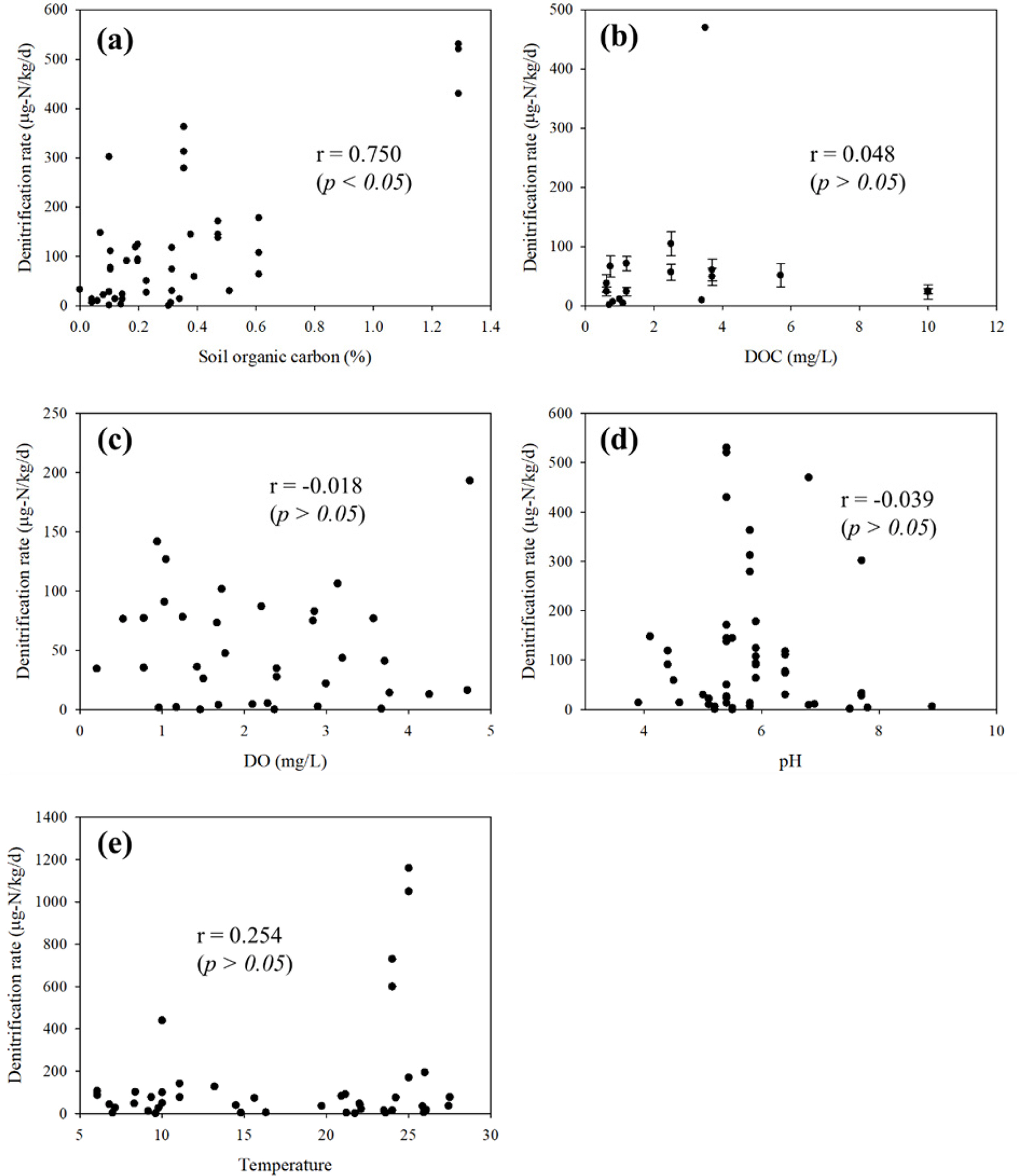
대상 현장의 지중환경 특성치와 탈질화 계수와의 상관관계를 파악하기 위해 각 문헌들에 제시된 다양한 지중환경 특성값들을 수집하고, 이에 따른 탈질화 계수 변화를 Fig. 2와 같이 도식화하였다. 이때, 탈질 반응은 일반적으로 환원환경에서 생물학적 반응에 의해 지배된다는 것에 착안하여(Jeon et al., 2020), 유기탄소 농도, 용존 산소 농도, pH, 온도 등, 혐기성 미생물 활성에 영향을 줄 수 있는 특성값들을 선정하여 탈질화 계수와의 상관성을 평가하였다. SPSS statistics 24 소프트웨어(SPSS Inc., Chicago, USA)를 사용하여 피어슨 상관계수(r)를 산정한 결과, 탈질화 계수는 토양 유기탄소 농도와 가장 큰 양의 상관관계를 보이는 것을 확인할 수 있었다(Fig. 2(a); r = 0.750, p < 0.05). 이는 질산성 질소의 탈질 반응이 주로 유기 탄소를 전자공여체로 이용하는 탈질 미생물들에 의해 일어나며(Devito et al., 2000; Pabich et al., 2001), 토양 유기탄소 농도가 높을수록 이러한 미생물들의 활성이 높아지기 때문인 것으로 판단된다. 하지만 토양 유기탄소와는 달리, 용존 유기탄소 농도는 상대적으로 탈질화 계수와 상관관계가 유의하게 나타나지 않았다(Fig. 2(b); p> 0.05). 탈질 미생물들은 비교적 용해도가 낮은, 큰 분자량의 유기탄소까지 탄소원으로 이용 가능한 것으로 알려져 있다(Barnes et al., 2012; De Catanzaro and Beauchamp, 1985). 즉, 탈질 미생물들이 토양입자 표면에 부착되어 성장하며 용존 유기탄소뿐 아니라, 일부 용해되지 않은 토양 유기탄소까지 효과적으로 이용 가능하기 때문에, 탈질화 계수가 용존 유기탄소 보다는 토양 유기탄소 농도와 더 상관관계가 높게 나타난 것으로 판단된다. 한편, 낮은 용존 산소 농도, 중성 pH, 25–30oC 범위의 온도 조건에서 탈질 반응이 활발히 일어난다고 서술하는 기존 문헌들(Robertson and Merkley, 2009; Xu et al., 2013)과는 달리, 용존 산소 농도, pH, 온도는 모두 탈질화 계수와 유의한 상관관계를 보이지 않았는데(Fig. 2(c), (d), (e); p > 0.05), 이는 앞서 제시한 토양유기탄소를 비롯해 민감도가 상대적으로 더 높은 인자의 영향이 복합적으로 작용했기 때문인 것으로 생각된다.
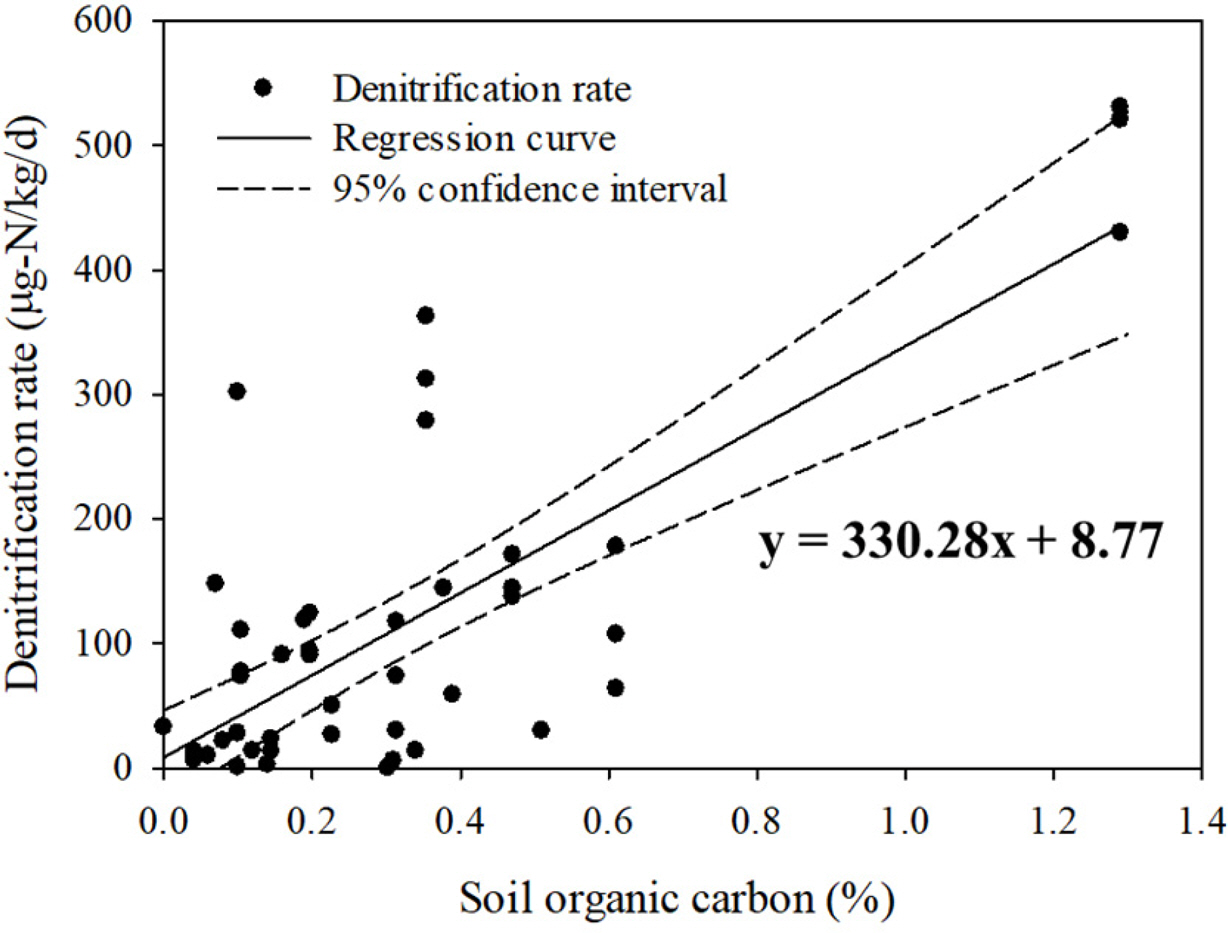
탈질화 계수는, 본 연구에서 조사한 다양한 지중환경 특성치 중, 유일하게 토양 유기탄소 농도와 통계적으로 유의한 상관관계를 보였다. 회귀분석 결과, 토양 유기탄소 농도(x, % w∙w-1)가 증가할수록 탈질화 계수(y, μg-N∙kg-1∙ d-1)도 증가하는, y = 330.28x + 8.77의 선형 관계를 나타내었다. 이러한 상관관계와 이에 대한 95% 수준 신뢰구간을 Fig. 3에 도식화하였다. 이를 통해, 질산성 질소 모델링 대상 부지 대수층 토양의 유기탄소 농도를 조사함으로써 비교적 간단하게 정확도 높은 부지특이적 탈질화 계수를 선정할 수 있을 것으로 보이며, 이에 따라 질산성 질소 모델링 결과의 신뢰성을 보다 향상시킬 수 있을 것으로 기대된다.
|
Fig. 1 Box plot with the maximum and minimum values of denitrification rates obtained from previous studies. |
|
Fig. 2 Denitrification rates versus various physicochemical properties of sites: (a) soil organic carbon, (b) dissolved organic carbon (DOC), (c) dissolved oxygen (DO), (d) pH, (e) temperature. r and p in the graph indicate the Pearson correlation coefficient and its pvalue, respectively. |
|
Fig. 3 Linear regression curve between denitrification rate and soil organic carbon content with its 95% confidence interval. |
본 연구에서는 지하수 질산성 질소 모델링 시 필요한 탈질화 계수를 효과적으로 선정하기 위한 방안에 대해 고찰하였다. 기존 문헌들에서 사용한 탈질화 계수 결정 방법들은 실질적인 수행에 있어 많은 비용이 들고 복잡하거나 혹은 모델링 결과의 정확도가 크게 떨어진다는 한계가 확인되었다. 현장 연구 기반의 문헌들을 조사하여 다양한 지중환경 특성과 탈질화 계수 간의 상관관계를 파악하고 관계식을 도출한 결과, 현장 토양의 유기탄소 농도와 탈질화 계수 간 높은 상관성을 확인할 수 있었다. 즉, 이 상관관계에 근거하여 부지특이적 탈질화 계수를 선정한다면 지하수 질산성 질소 모델링 결과의 신뢰성을 보다 향상시킬 수 있을 것으로 판단된다. 향후, 이 연구에서 제안된 방법으로 산정된 탈질화 계수를 적용하여 실제 질산성 질소 오염부지에 대해 모델링을 수행하고 그 예측치와 실제 관측값을 비교해 봄으로써 제안된 기법의 신뢰성을 검증하는 후속 연구가 필요할 것으로 판단된다.
본 연구는 환경부의 재원으로 한국환경산업기술원의 지중환경오염· 위해관리기술개발사업의 지원을 받아 수행되었습니다(2020002440002).
- 1. 석희준, 전철민, 2009, 농촌지역의 질산성질소 거동 해석을 위한 모델 개발 및 현장 적용, 자원환경지질, 42(6), 561-574.
- 2. 토양지하수정보시스템, https://sgis.nier.go.kr//web/contents/contentView/?pMENU_NO=109 [accessed 21.11.17.].
- 3. 환경부, 2021, 지하수의 수질보전 등에 관한 규칙, 환경부령 제942호.
- 4. Almasri, M.N. and Kaluarachchi, J.J., 2007, Modeling nitrate contamination of groundwater in agricultural watersheds, J. Hydrol., 343(3-4), 211-229.
-

- 5. Barnes, R.T., Smith, R.L., and Aiken, G.R., 2012, Linkages between denitrification and dissolved organic matter quality, Boulder Creek watershed, Colorado, J. Geophys. Res. Biogeosci., 117.
-

- 6. Birkinshaw, S.J. and Ewen, J., 2000, Nitrogen transformation component for SHETRAN catchment nitrate transport modelling, J. Hydrol., 230(1-2), 1-17.
-

- 7. Bonton, A., Rouleau, A., Bouchard, C., and Rodriguez, M.J., 2011, Nitrate transport modeling to evaluate source water protection scenarios for a municipal well in an agricultural area, Agric. Syst., 104(5), 429-439.
-

- 8. Böttcher, J., Strebel, O., Voerkelius, S., and Schmidt, H.L., 1990, Using isotope fractionation of nitrate-nitrogen and nitrate-oxygen for evaluation of microbial denitrification in a sandy aquifer, J. Hydrol., 114(3-4), 413-424.
-

- 9. Bradley, P.M., Fernandez Jr, M., and Chapelle, F.H., 1992, Carbon limitation of denitrification rates in an anaerobic groundwater system, Environ. Sci. Technol., 26(12), 2377-2381.
-

- 10. Burri, N.M., Weatherl, R., Moeck, C., and Schirmer, M., 2019, A review of threats to groundwater quality in the anthropocene, Sci. Total Environ., 684, 136-154.
-

- 11. Chowdary, V.M., Rao, N.H., and Sarma, P.B.S., 2004, A coupled soil water and nitrogen balance model for flooded rice fields in India, Agric. Ecosyst. Environ., 103(3), 425-441.
-

- 12. Chung, J., Chung, J.H., and Townsend, T.G., 2019, Approximation of transient redox boundary conditions: its application to numerical analysis of iron plume migration near landfills, Environ. Earth. Sci., 78, 711.
-

- 13. Clement, T.P., 1999, A modular computer code for simulating reactive multi-species transport in 3-dimensional groundwater systems, United States.
- 14. De Catanzaro, J.B. and Beauchamp, E.G., 1985, The effect of some carbon substrates on denitrification rates and carbon utilization in soil, Biol. Fertil. Soils, 1, 183-187.
-

- 15. Devito, K.J., Fitzgerald, D., Hill, A.R., and Aravena, R., 2000, Nitrate dynamics in relation to lithology and hydrologic flow path in a river riparian zone, J. Environ. Qual., 29(4), 1075-1084.
-

- 16. Dhakal, P., Matocha, C.J., Huggins, F.E., and Vandiviere, M.M., 2013, Nitrite reactivity with magnetite, Environ. Sci. Technol., 47(12), 6206-6213.
-

- 17. Francis, A.J., Slater, J.M., and Dodge, C.J., 1989, Denitrification in deep subsurface sediments, Geomicrobiol. J., 7(1-2), 103-116.
-

- 18. Frind, E.O., Duynisveld, W.H.M., Strebel, O., and Boettcher, J., 1990, Modeling of multicomponent transport with microbial transformation in groundwater: The fuhrberg case, Water Resour. Res., 26(8), 1707-1719.
-

- 19. Gu, C. and Riley, W.J., 2010, Combined effects of short term rainfall patterns and soil texture on soil nitrogen cycling - a modeling analysis, J. Contam. Hydrol., 112(1-4), 141-154.
-

- 20. Gupta, P.K., Kumari, B., Gupta, S.K., and Kumar, D., 2020, Nitrate-leaching and groundwater vulnerability mapping in North Bihar, India, Sustain. Water Resour. Manag., 6, 1-12.
-

- 21. Hansen, H.C.B., 1989, Composition, stabilization, and light absorption of Fe (II) Fe (III) hydroxy-carbonate (¡®green rust¡¯), Clay Miner., 24(4), 663-669.
-

- 22. Harrison, M.D., Groffman, P.M., Mayer, P.M., Kaushal, S.S., and Newcomer, T.A., 2011, Denitrification in alluvial wetlands in an urban landscape, J. Environ. Qual., 40(2), 634-646.
-

- 23. Huan, H., Hu, L., Yang, Y., Jia, Y., Lian, X., Ma, X., Jiang, Y., and Xi, B., 2020, Groundwater nitrate pollution risk assessment of the groundwater source field based on the integrated numerical simulations in the unsaturated zone and saturated aquifer, Environ. Int., 137, 105532.
-

- 24. Jahangir, M.M., Johnston, P., Addy, K., Khalil, M.I., Groffman, P., and Richards, K.G., 2013, Quantification of in situ denitrification rates in groundwater below an arable and a grassland system, Water Air Soil Pollut., 224, 1-14.
-

- 25. Jeon, J.-H., Lee, W.-C., Lee, S.-W., and Kim, S.-O., 2020, The effect of geological media on the denitrification of nitrate in subsurface environments, J. Soil Groundw. Environ., 25, 16-27.
-

- 26. Karanasios, K., Vasiliadou, I., Pavlou, S., and Vayenas, D., 2010. Hydrogenotrophic denitrification of potable water: A review, J. Hazard. Mater., 180(1-3), 20-37.
-

- 27. Koh, E.-H., Kaown, D., Mayer, B., Kang, B.-R., Moon, H.S., and Lee, K.-K., 2012, Hydrogeochemistry and isotopic tracing of nitrate contamination of two aquifer systems on Jeju Island, Korea, J. Environ. Qual., 41(6), 1835-1845.
-

- 28. Koh, E.-H., Lee, E., Kaown, D., Green, C.T., Koh, D.-C., Lee, K.-K., and Lee, S.H., 2018, Comparison of groundwater age models for assessing nitrate loading, transport pathways, and management options in a complex aquifer system, Hydrol. Process., 32(7), 923-938.
-

- 29. Koh, E.-H., Lee, E., and Lee, K.-K., 2016. Impact of leaky wells on nitrate cross-contamination in a layered aquifer system: Methodology for and demonstration of quantitative assessment and prediction, J. Hydrol., 541, 1133-1144.
-

- 30. Koh, E.-H., Lee, E., and Lee, K.-K., 2020, Application of geographically weighted regression models to predict spatial characteristics of nitrate contamination: Implications for an effective groundwater management strategy, J. Environ. Manage., 268, 110646.
-

- 31. Langergraber, G. and Šimůnek, J., 2005. Modeling variably saturated water flow and multicomponent reactive transport in constructed wetlands, Vadose Zone J., 4(4), 924-938.
-

- 32. Lasserre, F., Razack, M., and Banton, O., 1999, A gis-linked model for the assessment of nitrate contamination in groundwater, J. Hydrol., 224(3-4), 81-90.
-

- 33. Lee, M.-S., Lee, K.-K., Hyun, Y., Clement, T.P., and Hamilton, D., 2006, Nitrogen transformation and transport modeling in groundwater aquifers, Ecol. Model., 192(1-2), 143-159.
-

- 34. Lin, Y.-H. and Gu, Y.-J., 2020, Denitrification kinetics of nitrate by a heterotrophic culture in batch and fixed-biofilm reactors, Processes, 8(5), 547.
-

- 35. Lind, A.-M., 1983, Nitrate Reduction in the Subsoil, in Denitrification in the Nitrogen Cycle, edited by H. L. Goiterman,. Plenum, New York.
- 36. Meisinger, J. and Randall, G., 1991, Estimating nitrogen budgets for soil‐crop systems. In Managing nitrogen for groundwater quality and farm profitability, Soil Science Society of America, Inc. Madison Wisconsin, USA.
-

- 37. Morris, J.T., Whiting, G.J., and Chapelle, F.H., 1988, Potential denitrification rates in deep sediments from the southeastern coastal plain, Environ. Sci. Technol., 22(7), 832-836.
-

- 38. Pabich, W.J., Valiela, I., and Hemond, H.F., 2001, Relationship between doc concentration and vadose zone thickness and depth below water table in groundwater of cape cod, U.S.A. Biogeochemistry, 55, 247-268.
-

- 39. Poulsen, R., Cedergreen, N., Hayes, T., and Hansen, M., 2018, Nitrate: An environmental endocrine disruptor? A review of evidence and research needs, Environ. Sci. Technol., 52(7), 3869-3887.
-

- 40. Re, V., Sacchi, E., Kammoun, S., Tringali, C., Trabelsi, R., Zouari, K., and Daniele, S., 2017, Integrated socio-hydrogeological approach to tackle nitrate contamination in groundwater resources. The case of Grombalia Basin (Tunisia), Sci. Total Environ., 593-594, 664-676.
-

- 41. Robertson, W.D. and Merkley, L.C., 2009, In-stream bioreactor for agricultural nitrate treatment, J. Environ. Qual., 38(1), 230-237.
-

- 42. Senko, J.M., Dewers, T.A., and Krumholz, L.R., 2005, Effect of oxidation rate and Fe (II) state on microbial nitrate-dependent Fe (III) mineral formation, Appl. Environ. Microbiol., 71, 7172-7177.
-

- 43. Shamrukh, M., Corapcioglu, M.Y., and Hassona, F.A., 2001, Modeling the effect of chemical fertilizers on ground water quality in the Nile Valley Aquifer, Egypt, Groundwater, 39(1), 59-67.
-

- 44. Tilstra, A., El-Khaled, Y.C., Roth, F., Rädecker, N., Pogoreutz, C., Voolstra, C.R., and Wild, C., 2019, Denitrification aligns with N2 fixation in Red Sea corals, Sci. Rep., 9, 19460.
-

- 45. Van Rijn, J., Tal, Y. and Barak, Y., 1996, Influence of volatile fatty acids on nitrite accumulation by a Pseudomonas stutzeri strain isolated from a denitrifying fluidized bed reactor, Appl. Environ. Microbiol., 62, 2615-2620.
-

- 46. Wei, X., Bailey, R.T., Records, R.M., Wible, T.C., and Arabi, M., 2019, Comprehensive simulation of nitrate transport in coupled surface-subsurface hydrologic systems using the linked SWAT-MODFLOW-RT3D model, Environ. Model. Softw., 122, 104242.
-

- 47. Well, R., Augustin, J., Meyer, K., and Myrold, D., 2003, Comparison of field and laboratory measurement of denitrification and N2O production in the saturated zone of hydromorphic soils, Soil Biol. Biochem., 35(6), 783-799.
-

- 48. Xu, D., Li, Y., Howard, A., and Guan, Y., 2013, Effect of earthworm eisenia fetida and wetland plants on nitrification and denitrification potentials in vertical flow constructed wetland, Chemosphere, 92(2), 201-206.
-

 This Article
This Article
-
2021; 26(6): 74-81
Published on Dec 31, 2021
- 10.7857/JSGE.2021.26.6.074
- Received on Nov 24, 2021
- Revised on Nov 30, 2021
- Accepted on Dec 13, 2021
 Services
Services
- Abstract
1.서 론
2.질산성 질소 반응-이동 모델링을 위한 탈질화 계수 결정 방법
3.현장 특성을 고려한 부지특이적 탈질화 계수 선정 방안
4.결론 및 제언
- Acknowledgements
- References
- Full Text PDF
Shared
 Correspondence to
Correspondence to
- Seunghak Lee
-
1Water Cycle Research Center, Korea Institute of Science and Technology (KIST), Seoul 02792, Republic of Korea
2Division of Energy and Environmental Technology, KIST School, Korea University of Science and Technology (UST), Seoul 02792, Republic of Korea
3Graduate School of Energy and Environment (KU-KIST Green School), Seoul 20841, Republic of Korea - E-mail: jschung@kist.re.kr