- Recovery of Lead and Zinc from Lead-Zinc Mine Tailings Using a Fuel Cell-Based Leaching System
Won Jung Ju and Kyoungphile Nam*
Department of Civil and Environmental Engineering, Seoul National University, Seoul 08826, Korea
- 연료전지 기반 침출 시스템을 이용한 납·아연 광산 광미 내 납·아연 회수 연구
주원정ㆍ남경필*
서울대학교 건설환경공학부
This article is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Mine tailings, fine-grained residues from ore beneficiation, contain substantial unrecovered metals such as lead(Pb) and zinc(Zn). These metals are vital for industry, and Pb is listed among Korea’s ten strategic critical minerals. This study aimed to maximize the leaching of Pb and Zn and developed a fuel cell-based leaching system to simultaneously recover metals and generate electricity using Pb-Zn mine tailings as the anode active material. The single-chamber fuel cell, composed mainly of quartz, pyrite, dolomite, and chlorite-serpentine, served as both an electron source and a leaching substrate. The physical separation of anodic oxidation and cathodic oxygen reduction enabled sustained oxidation of tailings in the anode, suppressing surface passivation and promoting electron transfer. The system achieved a maximum power density of 5.4 mW/m2 at 43.8 mA/m2 and 0.11 V. Under a 300 Ω external load, the closed-circuit voltage remained at about 8.5 mV for ten days. During operation, 37.3 mg-Pb/kg and 84.2 mg-Zn/kg were leached, corresponding to efficiencies of 1.4% and 0.6%, equivalent to annual leaching rates of approximately 50%/yr and 20%/yr, respectively. These results indicate that galvanic interactions between pyrite and base-metal sulfides, combined with the lower rest potential of PbS, enhanced Pb dissolution. When scaled up to a 1 m2 module (20 × 20 unit cells), the system produced 6.0 mW (2 V), and application to a 20,900 m2 tailings dam was estimated to yield 125 W total output. The proposed self-sustaining system enables continuous electricity generation and metal recovery through sulfide oxidation, providing a sustainable approach to mitigate environmental risks and promote resource circularity in mine waste management.
Keywords: Fuel cell, Metal recovery, Electricity generation, Sulfidic mine tailings, Galvanic leaching
광미(mine tailings)는 광석을 정광으로 분리하는 과정에서 발생하는 100 μm 이하의 미세 입자 형태의 부산물로, 전 세계적으로 회수되지 못한 금속이 대량으로 축적되어 있는 인공 자원 저장소로 평가된다(Park et al., 2019). 일반적으로 채굴된 광석의 약 97-99%가 정광 회수 후 폐기되는 것으로 알려져 있으며, 이러한 광미에는 과거의 기술적·경제적 한계로 인해 유용 금속이 상당량 잔존한다(USGS, 2018; Adiansyah et al., 2015).
Mudd (2017)는 전 세계 67개국의 851개 납·아연 광상 및 광산 폐기물을 대상으로 데이터베이스를 구축하였으며, 이를 통해 총 2억 2,610만 톤의 납과 6억 1,030만 톤의 아연이 평균 품위 0.44% 납 및 1.20% 아연 형태로 존재함을 보고하였다. 이러한 결과는 현재 가동 중인 광상뿐 아니라 과거 채굴 및 제련 활동으로 축적된 광미 내에도 상당한 양의 납과 아연 자원이 잔존하고 있음을 의미한다. 즉, 광산 폐기물은 단순한 환경 오염원이 아니라, 재활용 가능한 지상 광산(above-ground mines)으로서 잠재적 자원 가치를 지니고 있음을 시사한다.
또한, USGS(2024)의 Mineral Commodity Summaries에 따르면 납과 아연의 평균 시장 가격은 각각 2.53 USD/kg 및 1.52 USD/kg로 보고되었다. 이는 광미 내 잔존 금속의 경제적 가치가 여전히 높음을 보여주며, 광산 폐기물의 자원화가 환경적 측면뿐 아니라 경제적 측면에서도 충분히 유의미한 대안이 될 수 있음을 뒷받침한다. 특히 납(Pb)은 우리나라에서 지정한 10대 전략 핵심광물 중 하나로 분류되며(Table 1), 산업 전반에서 필수 소재로 사용된다.
최근 1차 자원의 고갈과 광미 적치장으로부터 유발되는 환경 위해성에 대한 우려가 증대되면서, 폐광미로부터 납과 아연을 회수하기 위한 다양한 기술이 활발히 연구되고 있다. 대표적인 재처리 기술로는 화학적 침출(Hussaini et al., 2021; Khalil et al., 2025), 미생물 침출(Ye et al., 2017; Rouchalova et al., 2020), 전기동력학적 침출 (Chen et al., 2024) 등이 있다. 그러나 이러한 방법들은 과도한 시약 사용, 부반응 생성물에 의한 피동화, 높은 에너지 소모 등 다양한 한계를 지니고 있어, 이를 극복할 수 있는 지속 가능한 금속 회수 기술의 개발이 필요하다.
이에 본 연구에서는 이러한 한계를 보완하기 위해 연료전지 기반 침출 시스템(fuel cell-based leaching system)을 적용하여 납·아연 광산 광미 내 황화광물을 산화시키면서 납과 아연을 회수하고 동시에 전력을 생산할 수 있는 새로운 기술적 접근을 제안하였다. 제안된 시스템에서 납·아연 광미의 산화 반응은 음극에서 일어나며, 방출된 전자는 외부 회로를 통해 양극의 환원 반응을 유도함으로써 전기가 생성된다(Ju et al., 2018; Ju et al., 2025). 본 연구는 연료전지 기술을 활용한 광미 산화가 환경 정화와 유용 금속 회수를 동시에 달성할 수 있음을 실험적으로 검증하였다. 또한 전기 생산과 금속 회수 효율을 극대화할 수 있는 시스템 설계 지침을 제시하고, 납·아연 광산 광미 적치장에 적용했을 때의 현장 적용성도 평가하였다. 이러한 결과는 연료전지 기반 침출 기술이 기존 처리 방법에 비해 더 친환경적이고 지속가능한 대안이 될 수 있음을 입증한다.
|
Table 1 Selected critical minerals among major countries (Korea, the United States, Japan, the EU, and the IEA)(Kim, 2024) |
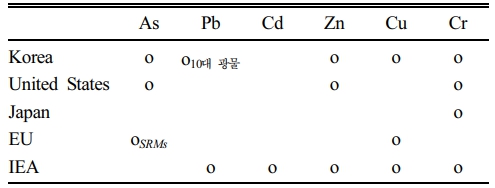
한국의 “10대 광물”은 10대 전략 핵심광물을, EU의 “SRMs”는 strategic raw materials를 의미 |
2.1. 납·아연 광산 광미 시료 채취
실험에 사용된 광미 시료는 경상북도 봉화에 위치한 가동 중인 납·아연 광산에서 2014년 12월에 채취했다. 채취한 시료는 자연 건조 후 풍화 및 산화 과정을 최소화하기 위해 밀폐 용기에 보관한 후 실험에 사용했다.
2.2. 납·아연 광산 광미의 광물학적 및 화학적 특성 분석
광미의 결정 구조는 X선 회절분석기(XRD, D8 Advance, Bruker, Germany)를 이용하여 분석하였다. 분석 조건은 40 kV, 30 mA에서 구리(Cu) 타깃을 사용하였으며, 2Θ = 2.0°~70.0°범위에서 0.02°간격으로 측정했다.
광미 내 잔류 중금속 함량은 미국 USEPA에서 제시한 EPA 3052 방법(USEPA, 1996)을 이용하여 측정했다. 약 0.5 g의 시료를 테플론 용기에 넣고, 9 mL HNO3, 3 mL HF, 2 mL HCl, 1 mL H2O2혼합 산용액을 가하여 Microwave(MARS 6 230/60, CEM, USA)를 이용해 180°C까지 5.5분간 승온 후 9.5분간 유지하였다. 분해 후 시료는 실온에서 냉각하고 0.45 μm GHP syringe filter로 여과하여 분석에 사용했다.
광미 내 금속의 결합 형태는 Tessier et al.(1979)이 제시한 연속추출법을 이용하여 확인하였다. 교환성 금속(Exchangeable; Tessier F1)은 1 M MgCl2용액(pH 7.0)을 사용하여 추출하였으며, 탄산염 결합형(Carbonate-bound; Tessier F2) 금속은 1 M sodium acetate 용액(pH 5.0, acetic acid로 조정)을 사용하여 추출하였다. Fe 및 Mn 산화물 결합형(Fe/Mn oxide-bound; Tessier F3) 금속은 25% acetic acid 용액 내 0.04 M NH2OH·HCl을 사용하여 추출하였다. 각 단계에서 추출된 용액은 0.45 μm GHP syringe filter로 여과한 후 As, Pb, Cd, Zn, Cu, Ni, Fe, Cr, S 등의 농도를 분석하였다.
광미의 중금속 침출 가능성은 한국 폐기물공정시험기준(STM)(KMOE, 2014a)에 따라 평가하였다. 체거름(2 mm 통과)한 시료 100 g을 증류수(pH 5.8~6.3, HCl로 조정)와 1:10 비율로 혼합한 뒤 200 rpm에서 6시간 동안 교반하였으며, 이후 원심분리기에서 12,000 g로 15분간 분리하였다. 상등액은 0.45 μm GHP syringe filter로 여과하여 분석하였다. 미국 독성특성용출법(Toxicity Characteristic Leaching Procedure, TCLP)를 적용하여 산성 조건에서의 금속 용출 특성을 평가하였다(USEPA, 1992). TCLP(pH 4.93)은 acetic acid 5.7 mL/L와 1 N NaOH 64.3 mL/L로 조정된 용액(약 pH 4.93)을 용출액으로 사용하였으며, TCLP(pH 2.88)은 5.7 mL/L acetic acid 용액(약 pH 2.88)을 용출액으로 사용하였다. 두 조건 모두에서 시료와 용출액을 1:20의 고상:액상 비율로 혼합한 뒤, 200 rpm에서 18시간 동안 회전식 교반기에서 교반하였다. 이후 12,000 g에서 15분간 원심분리하여 상등액을 분리하였으며, 0.45 μm GHP syringe filter로 여과한 후 As, Pb, Cd, Zn, Cu, Cr 등의 농도를 분석하였다.
2.3. 침출액 및 수질 분석
총함량 분석, 연속추출, 용출시험에서 얻어진 추출액 및 침출액 내 금속(As, Pb, Cd, Zn, Cu, Ni, Fe, Cr)과 S 농도는 유도결합플라즈마 분광광도계(Inductively Coupled Plasma Optical Emission Spectrometry; ICP-OES)(ICAP 7400 DUO, Thermo Scientific, USA)를 이용하여 측정하였다. 검출한계는 Cr 0.010, Fe 0.007, Ni 0.0134, Cu 0.005, Zn 0.004, As 0.089, Cd 0.015, Pb 0.065, S 0.090 mg/L이었다.
용존산소(DO), 산화환원전위(Eh), 수소이온농도(pH)는 Orion 5-star portable meter(Thermo Fisher Scientific)를 이용하여 측정하였다. 수용액 내 Fe2+ 및 Fe3+ 농도는 ferrozine 방법(Viollier et al., 2000)으로 분석하였다.
2.4. 연료전지 구성 및 운전조건
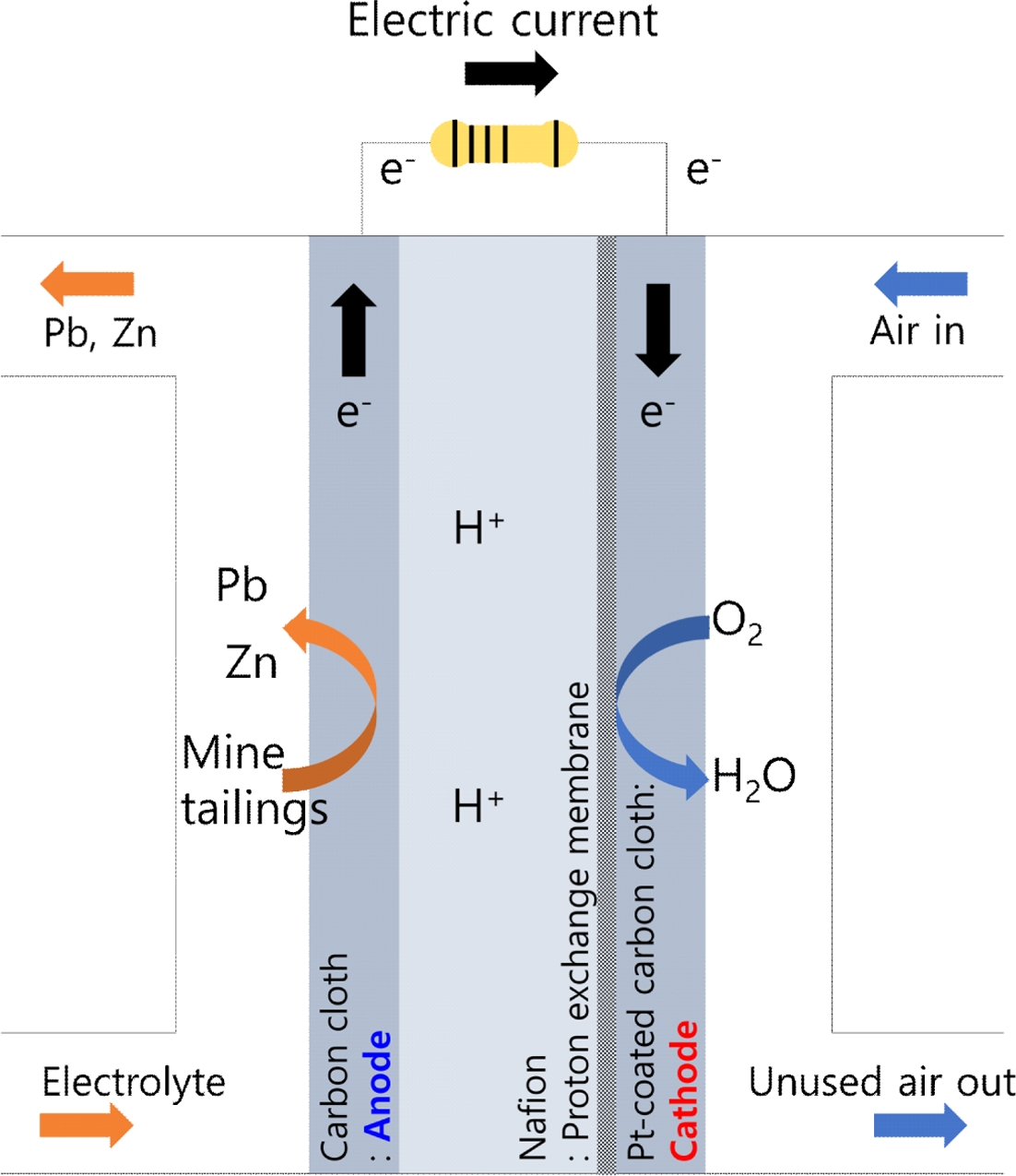
Fig. 1은 연료전지 기반 침출 시스템을 이용한 납·아연 회수 모식도를 나타낸다. 연료전지는 Plexiglas를 이용하여 단일 챔버형 공기-음극 연료전지로 제작하였으며, 전체 부피는 125 mL(5 × 5 × 5 cm)였다. 상부에 설치된 두 개의 포트는 시료 채취 및 기준 전극 삽입용으로 사용되었으며, 실험 시 고무마개로 밀폐하였다. 전극은 Carbon cloth(Ballard, USA, 두께 0.35 mm)를 양극으로, Nafion 117(Dupont, USA)을 양이온 교환막으로, 그리고 0.5 mg/cm2 Pt 촉매가 도포된 carbon cloth를 음극으로 구성하였다. 전극은 140°C, 20 MPa 조건에서 3분간 열압착하여 Membrane electrode assembly(MEA)를 제작하였다. 양극 전극(Carbon cloth)과 음극 전극(촉매가 도포된 carbon cloth)은 Pt wire로 외부 저항을 연결하였으며, 발생 전압은 Keithley 2700 multimeter (USA)를 이용해 20분 간격으로 측정하였다. 전해질은 기존 보고된 9K 배지에서 철 성분을 제외한 0K 배지를 사용하였다. 이 용액은 (NH4)2SO4 3.0 g/L, KCl 0.10 g/L, K2HPO4 0.50 g/L, MgSO4·7H2O 0.50 g/L, Ca(NO3)2 20.01 g/L, H2SO4 1 mL/L (10 N)을 포함하였다.
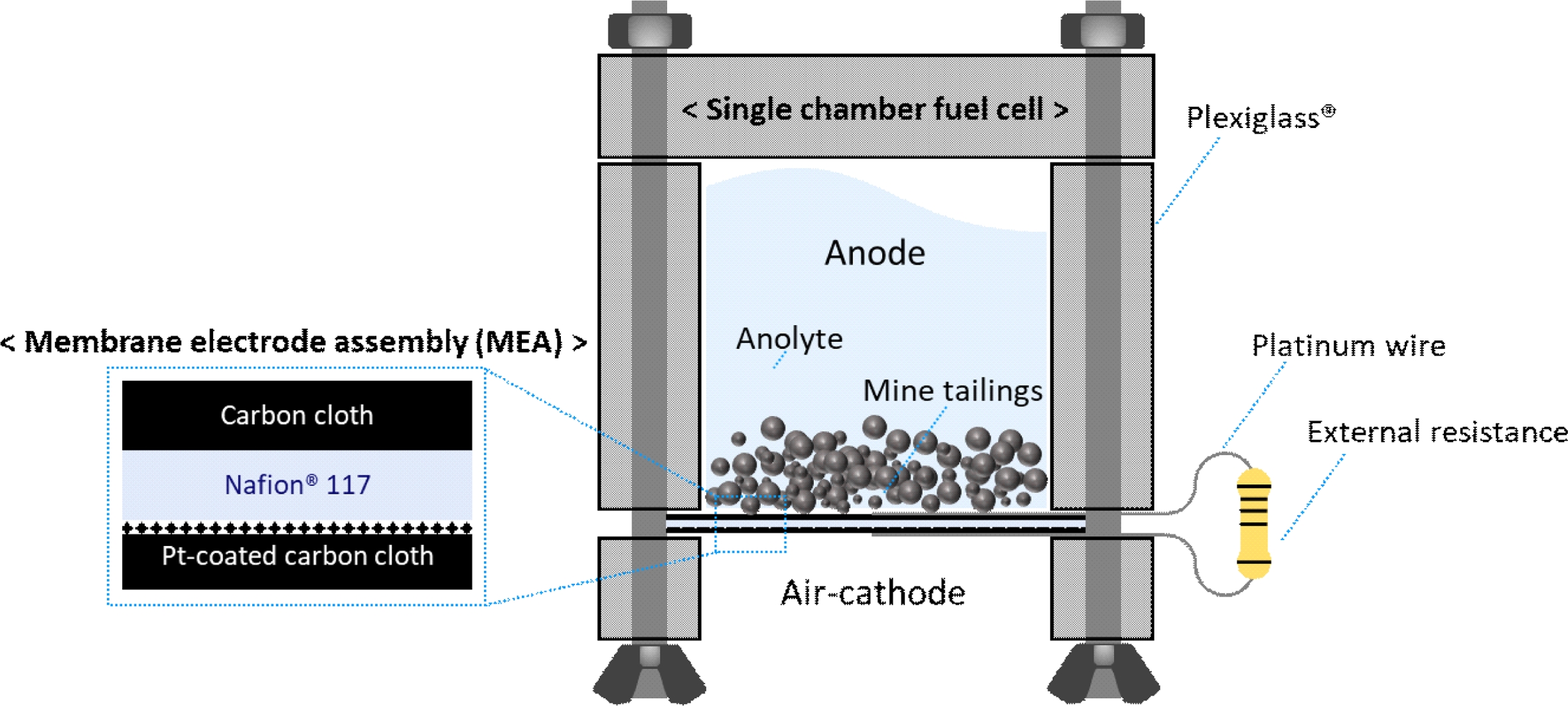
연료전지의 구성은 Ju et al.(2025)와 같으며, 평균 입경 60 μm 이하의 광미 시료 10 g을 0K 전해질(100 mL)과 함께 연료전지 음극부(Anode)에 충진했다(Fig. 2). 광미는 MEA의 carbon cloth 부분과 고르게 접촉되도록 하여 운전했다.
2.5. 연료전지 출력 특성 분석: 방전 시험(Discharging test)
연료전지에서 발생하는 전자의 방출 특성은 전류밀도-전압(I-V) 곡선과 전류밀도-전력밀도(I-P) 곡선을 통해 평가하였다. 외부저항을 10~10,000 Ω 범위에서 큰 값에서 작은 값의 순으로 단계적으로 연결하였으며, 각 저항 조건에서의 전압은 Keithley 2700 multimeter(USA)를 이용해 측정했다. 측정된 전압 데이터를 바탕으로 전류밀도(I)와 전력밀도(P)를 계산하였다. 전류밀도는 측정된 전압을 외부저항과 양극 면적으로 나눈 값으로 산출하였으며, 전력밀도는 전압의 제곱을 외부저항과 양극 전극 면적으로 나눈 값으로 계산하였다.
|
Fig. 1 Schematic diagram of lead and zinc recovery using the fuel cell-based leaching system. |
|
Fig. 2 Schematic of mine tailings-fuel cell. |
3.1. 납·아연광산 광미의 물리·화학적 특성
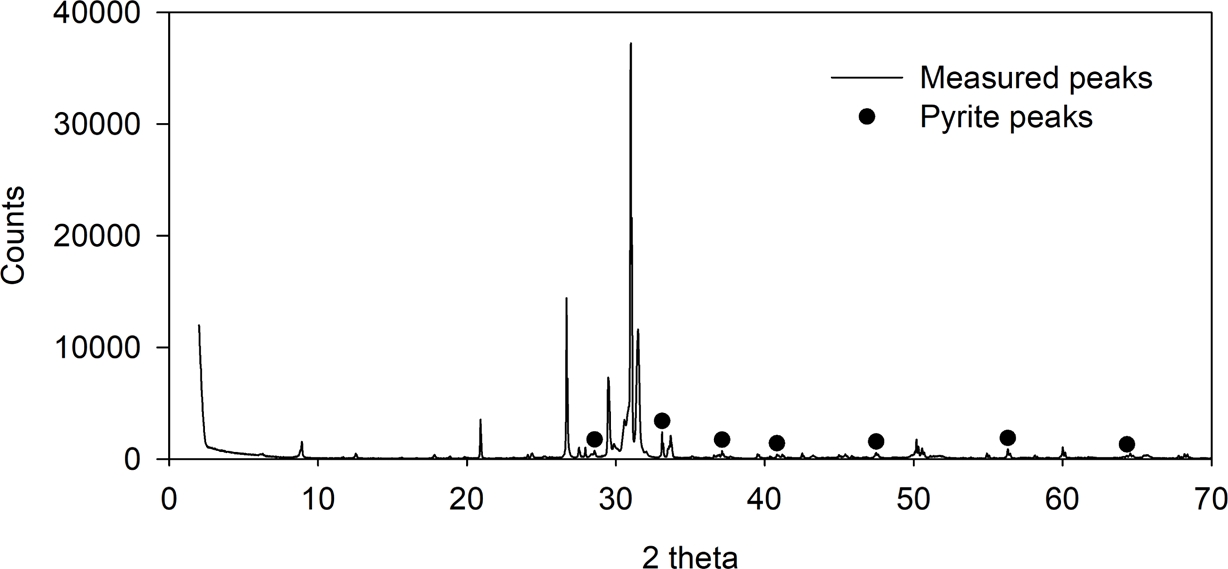
XRD 분석 결과(Fig. 3), 납·아연광산 광미는 석영(SiO2), 황철석(pyrite; FeS2), 돌로마이트(Dolomite; CaMg(CO3)2), 일라이트(Illite; (K,H3O)(Al2Si3AlO10)(OH)2), 녹니석(Chlorite-surpentine; (Mg,Al)6(Si,Al)4O10(OH)8) 등의 규산염 및 탄산염 광물이 주성분으로 확인되었다. 또한 부틀러라이트(Butlerite; (Fe3+SOO4(OH)·H2O)와 구리-철 황화광물(Cu6(Cu0.48Fe5.52)As4S13) 등이 동정되어, 광미 내 일부 황화광물이 이미 산화 과정을 거쳐 2차 황산염 및 금속 황화물로 전환되었음을 시사한다.
이러한 광물 조성은 황철석과 구리-철 황화광물과 같은 황화광물이 산화될 때 산성 용액과 황산염을 형성하여 산성광산배수(acid mine drainage, AMD)를 유발할 수 있는 한편, 이 과정에서 납, 아연, 구리 등 다량의 금속 이온이 침출되므로 금속 회수 잠재성 또한 동시에 내포하고 있다. EPA 3052 방법을 통한 전함량 분석(Table 2) 결과에 따르면, 광미에는 납 2,671±15 mg/kg, 아연 14,851±541 mg/kg이 존재하는 것으로 나타났으며, 비소, 카드뮴, 구리, 크롬 등 다른 금속 또한 상당한 농도로 검출되었다. 이는 광미가 환경 위해성을 갖는 동시에, 특히 납과 아연의 함량이 높아, 광미가 환경오염원의 잠재성과 동시에 금속 회수 자원으로서의 가치를 갖는 것으로 판단된다.
Tessier 연속추출법 결과(Table 2), 아연은 교환성(Tessier F1) 및 철/망간 산화물(Tessier F3)에서 뚜렷하게 검출되어 비교적 용출이 용이한 형태로도 존재하는 반면, 납은 주로 철/망간 산화물 결합형(Tessier F3)에 집중되어 있어 상대적으로 안정적인 형태임을 확인하였다. 이러한 금속의 결합 특성은 연료전지 기반 전기화학적 침출 과정에서 금속별 용출 거동 차이를 설명하는 중요한 근거가 된다.
따라서, 납·아연광산 광미는 비활성적인 석영이 모재를 구성하는 동시에, 광미 내 황철석과 구리-철 황화광물이 산화되어 전자를 방출함으로써 연료전지의 전류 발생에 기여하고, 동시에 금속 이온을 침출시키는 반응원으로 작용한다. 이러한 광물학적 특성은 연료전지 기반 침출 시스템의 금속 회수 효율과 전기 생산 안정성에 직접적인 영향을 미치는 것으로 판단된다.
3.2. 납·아연 광미 연료전지 시스템의 전력 출력 특성
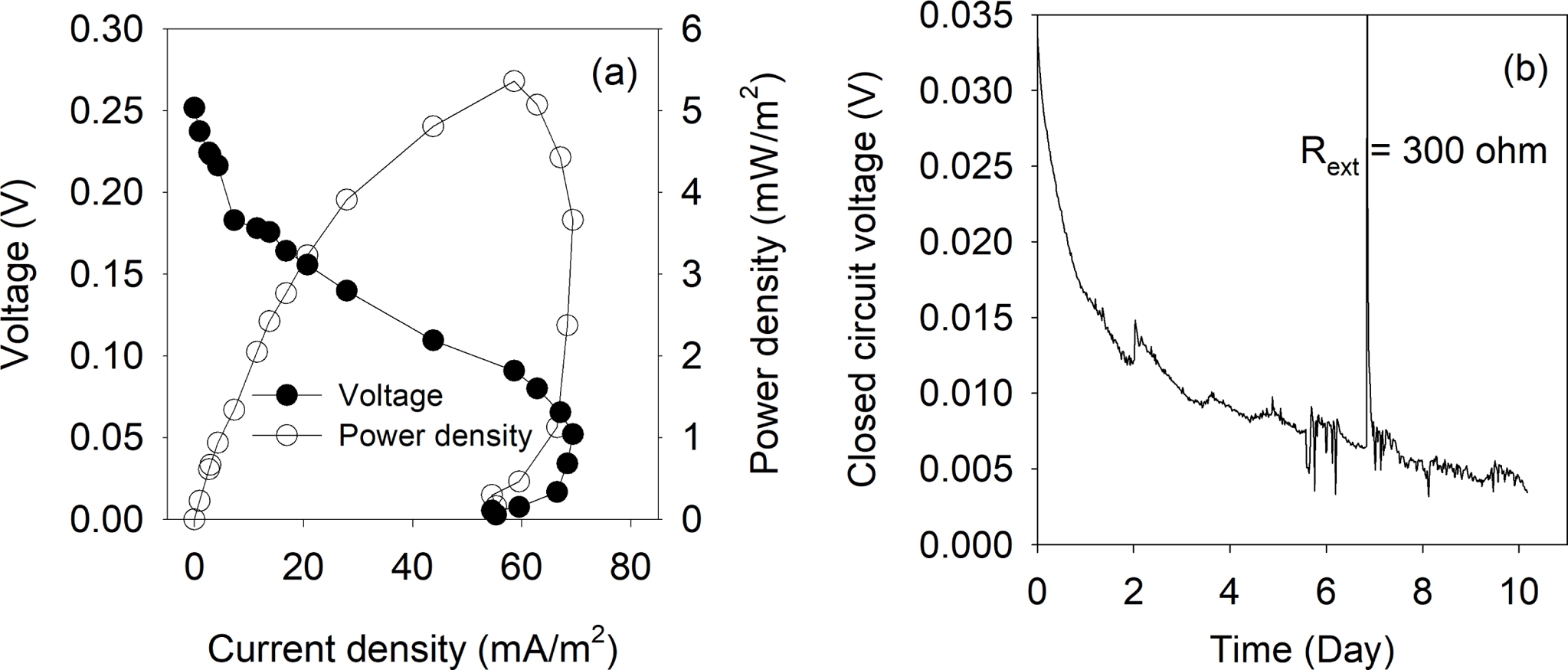
방전 시험 결과(Fig. 4(a)), 납·아연 광미 연료전지는 전류밀도 43.8 mA/m2, 전압 0.11 V에서 전력밀도 5.4 mW/m2를 기록하였다. 최대 전력 출력은 전류밀도 69.4 mA/m2에서 나타났으며, 이에 따라 최대 출력 지점에 해당하는 외부 저항 300 Ω을 설정하여 광미로부터 납과 아연의 침출을 유도하였다. 납·아연 광미를 장전한 단일 챔버형 연료전지를 해당 조건에서 10일간 운전한 결과, 평균 폐회로 전압은 약 8.5 mV로 유지되었다(Fig. 4(b)).
본 연구에서 얻어진 최대 전력밀도(5.4 mW/m2)는 기존에 보고된 황철석 기반 연료전지의 출력 범위와 유사한 수준을 보인다. 예를 들어, Ge et al.(2020)은 황철석을 음극 활성물질로 사용한 constructed wetland microbial fuel cell(PCW-MFC)에서 최대 전류밀도 47.77 mA/m2 및 전력밀도 6.74 mW/m2를 보고하였으며, Yan et al.(2021)은 유사한 시스템에서 27.8 mW/m2를 기록하였다. 따라서, 납·아연 광미를 활용한 본 연료전지는 상용 황철석 연료전지와 비교해도 경쟁력 있는 출력 수준을 갖는 것으로 평가된다. 이는 광미 내 황철석이 전자공급원으로 작용하여 전류생성에 기여했기 때문으로 판단된다.
3.3. 납·아연 광미 연료전지 시스템의 금속 침출 특성
연료전지 기반 침출 실험에서 납·아연 광미로부터의 금속 침출 거동을 평가한 결과(Table 3), 10일간의 운전 동안 납은 37.0 mg/kg, 아연은 84.3 mg/kg이 침출되었다. 이는 초기 함량 2,671 mg-Pb/kg 및 14,851 mg-Zn/kg을 기준으로 각각 1.4%와 0.6%의 침출율에 해당한다. 이러한 침출율을 연간 기준으로 환산하면 납은 약 50%/year, 아연은 약 20%/year로 계산되었으며, 이는 기존의 힙리칭(heap leaching) 공정과 유사한 수준이다. 예를 들어 Lizama (2003)는 힙리칭 조건에서 아연의 연간 침출율을 대략 40%로 보고한 바 있으며, 본 연구에서 제안하는 연료전지 기반 시스템은 이와 비교해도 경쟁력이 있음을 확인할 수 있다.
연료전지 운전 조건에서 얻어진 침출액의 pH는 5.95±0.072, 산화환원전위(Eh)는 425.6±3.4 mV로 측정되었으며, 전기전도도는 9.50±0.41 mS/cm였다. 이러한 pH-Eh 조건은 황화광물의 산화와 금속 침출에 중요한 영향을 미친다. 황철석(pyrite; FeS2)의 휴지전위는 약 0.63 V, 방연석(galena; PbS)은 0.28 V, 섬아연석(sphalerite; ZnS)은 0.24 V로 보고되어 있다(Li et al., 2013). 본 실험에서 측정된 Eh는 0.43 V 수준으로, 방연석의 휴지전위(0.28 V)를 충분히 초과하여 납의 산화와 용출이 가능한 영역에 해당한다. 반면 섬아연석의 휴지전위(0.24 V)와 비교했을 때, 아연 역시 열역학적으로 침출이 가능하나, Pb에 비해 상대적으로 낮은 침출율을 보였다. 이는 아연이 철/망간 산화물 결합형(Tessier F3)으로 안정적으로 존재하는 비율이 높아, 단순한 산화 조건만으로는 용출이 제한되었기 때문으로 해석된다.
납·아연 광산 광미 내 황철석의 존재는 전자 전달의 매개체로서 중요한 역할을 수행한다. 황철석은 높은 전기화학적 전위를 가지며, 전위가 낮은 방연석이나 섬아연석으로부터 전자를 받아들임으로써 이들의 산화를 촉진한다. 이러한 갈바닉 상호작용(galvanic interaction)은 다종의 황화광물이 공존하는 시스템에서 산화 및 금속 침출 속도를 크게 증가시키는 것으로 알려져 있다(Chopard et al., 2017; Qian et al., 2018; Aikawa et al., 2020). 실제로 황철석 존재할 경우 방연석와 섬아연석의 산화가 각각 단독 존재 조건보다 훨씬 빠르게 진행되며, 이는 산성광산배수 형성 과정에서도 관찰되는 현상이다.
연료전지 기반 시스템의 경우, 이러한 자연적 갈바닉 반응이 외부 회로로 연결된 전자 전달 경로를 통해 지속적으로 유지된다는 점에서 기존의 화학적 침출과 근본적인 차이를 가진다. 산화 반응에서 방출된 전자는 음극(anode)에서 외부 회로를 따라 양극(cathode)으로 이동하여 산소 환원 반응을 유도하고, 다시 산화환원 순환(redox cycling)을 지속시킨다. 이와 같은 전자 순환은 황화광물 표면에 형성될 수 있는 피막(passivation)을 억제하고, 광미 내 산화 환경을 장기적으로 안정화시켜 금속 침출의 지속성을 확보한다.
또한 황화광물의 산화 과정에서 생성된 수소 이온(H+)는 비전도성 금속 함유 광물의 용해를 촉진하고, 비소, 납, 아연 등의 이동성을 증가시킨다(Yang et al., 2009). 이러한 반응 메커니즘은 본 연구의 연료전지 시스템이 산성광산배수를 직접적으로 저감하기보다는, 금속을 용해된 형태로 회수하여 자원화하는 데 초점을 둔 기술임을 시사한다.
한편, Pb와 Zn 외에 침출액 내 공존금속으로 Fe 0.5 mg/L, Al 0.2 mg/L가 소량 검출되었다. 이는 광미 내 점토광물(예: illite, chlorite) 및 철-산화물상의 제한적 용해에 기인한 것으로 보인다. 본 시스템의 운전 조건은 pH 5.0–6.0, Eh 0.30–0.44 V로 유지되었으며, 이 전위-pH 구간은 PbS(방연석)의 휴지전위(≈0.28 V)를 상회하고 ZnS(섬아연석)의 휴지전위(≈0.24 V)와 유사한 영역에 해당하여 Pb > Zn 순의 침출 개시가 열역학적으로 유리한 조건이다. 반면 Fe는 동일 pH에서 Fe(III) 수산화물의 형성/침전이 우세하고, 생성된 고체상에의 흡착–공침(co-precipitation) 가능성으로 인해 용액 내 농도가 낮게 유지된 것으로 해석된다.
본 연구의 연료전지 기반 침출 시스템은 광미 내 황철석의 자발적 산화반응을 이용하여 Pb 및 Zn의 침출을 극대화하는 것을 목표로 한다. 이 과정에서 생성된 침출액(leachate)은 금속 회수를 위한 전처리 용액(feed solution)으로 활용될 수 있으며, Pb·Zn과 함께 소량의 Fe, Al, As 등이 공존한다. 이러한 금속들은 후속 공정에서의 중화(neutralization), 전기화학적 회수(electrochemical recovery), 또는 선택적 침전(selective precipitation)을 통해 단계적으로 회수될 수 있다. 나아가 본 시스템은 황화광물 간의 자연적 갈바닉 반응을 전기화학적으로 활용하여 금속 침출과 전력 생산을 동시에 달성하는 자가발전형 침출 공정(self-powered leaching process)으로, 기존의 화학적 침출 방식보다 환경부하가 낮고 에너지 효율이 높은 지속가능한 자원 회수 대안으로 제시될 수 있다.
3.4. 현장 적용 시나리오
본 연구에서 개발한 단일 챔버형 연료전지를 납·아연 광미 적치장 현장에 적용하는 경우를 가정하였다. 현장 조사 결과, 대상 광미 적치장의 면적은 약 110 m × 190 m로 총 20,900 m2이었다.
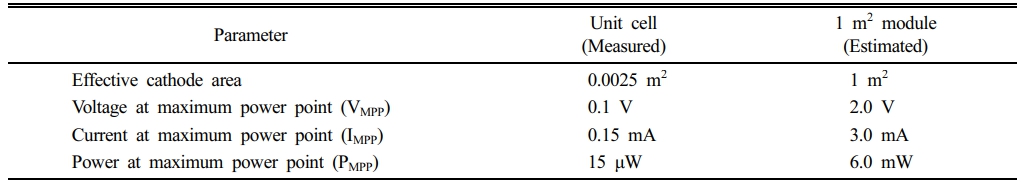
단일 챔버형 연료전지를 모듈화하여 전체 적치장 면적을 덮도록 확장하였으며 이 때의 예상 출력량을 산정했다(Table 4). 각 1 m2 모듈은 20개 직렬 × 20개 병렬로 연결된 총 400개의 단위 셀(unit cell)로 구성되며, 2 V에서 약 6 mW의 출력을 생성한다. 이를 전체 면적에 적용할 경우, 시스템 전체 출력은 약 125 W(2 V 기준)에 달한다. 이 출력은 30 W LED 가로등 네 개를 지속적으로 구동할 수 있는 수준으로, 별도의 외부 전력 공급 없이도 현장 내 조명 및 저전력 센서 운용이 가능하다. 동시에 연료전지 반응을 통해 광미 내 납과 아연의 침출이 촉진되며, 약 2년의 운전 기간 동안 완전한 침출이 달성될 것으로 예상된다. 따라서 본 시스템은 광미 내 유용 금속을 회수함과 동시에 전기를 생산할 수 있다는 점에서, 에너지 자립형 자원회수 기술로서의 의의가 크다.
|
Fig. 3 XRD analysis results of the Pb-Zn mine tailings used in this study |
|
Fig. 4 Power generation and discharging performance of a Pb-Zn mine tailings fuel cell. (a) Discharging test results of the fuel cell operated at 23°C. (b) Closed-circuit voltage under an external resistance of 300 Ω over 10 days. |
|
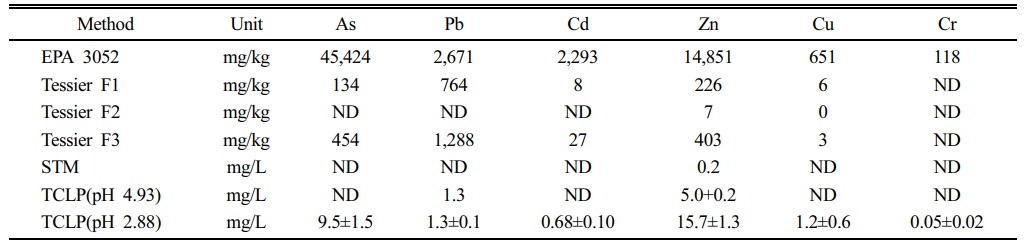
Table 2 Total contents (EPA 3052), chemical fractionation (Tessier F1, F2, F3), and leaching characteristics (STM, TCLP) of heavy metals in the Pb–Zn mine tailings |
|
Table 3 Concentrations of metals leached from Pb-Zn mine tailings after 10 days of operation using the fuel cell-based leaching system |

|
Table 4 Comparison of the unit cell and 1 m2 module performance of the Pb-Zn mine tailings fuel cell (module estimated based on the unit cell performance; 20 in series × 20 in parallel) |
본 연구에서는 납·아연 광산 광미를 연료로 활용하여 전기 생산과 금속 회수를 동시에 수행할 수 있는 연료전지 기반 침출 시스템을 제안하였다. 광미는 석영(SiO2), 황철석(FeS2), 돌로마이트(CaMg(CO3)2) 등으로 구성되어 있으며, 이 중 황철석과 같은 황화광물이 산화되면서 전자를 방출하여 연료전지의 전류 발생과 금속 침출에 기여하였다. 광미에 포함된 황화광물의 조성은 모광상의 특성에 따라 달라지며, 일반적으로 황철석(FeS2)이 우세하고, 황동석(CuFeS2), 황비철석(FeAsS), 방연석(PbS), 섬아연석(ZnS) 등이 함께 존재한다. 이러한 황화광물들은 광미의 산화, 금속 용해, 그리고 연료전지 응용에서의 전기 생산에 핵심적인 역할을 수행한다. 여러 황화광물이 공존할 경우, 갈바닉 상호작용(galvanic interaction)이 산화 및 용해 거동에 중요한 영향을 미친다. 상대적으로 높은 전위의 황철석은 섬아연석(ZnS)이나 방연석(PbS)으로부터 전자를 받아들여 이들의 산화를 촉진시키며, 전이된 전자는 연료전지의 음극으로 이동하여 전류를 생성한다. 이와 같은 반응은 황철석이 존재할 때 금속 침출 속도를 가속화하고, 연속적인 전자 이동을 통해 산화환원 순환을 유지시킨다. 또한 황화광물의 산화 과정에서 발생한 양성자는 금속 함유 광물의 용해를 촉진하여 비소, 납, 아연 등의 이동성을 증가시키는 데 기여한다. 연료전지 시스템의 가장 큰 특징은 음극(광미의 산화)과 양극(산소의 환원)이 물리적으로 분리되어 음극에 주입된 광미의 산화가 지속적으로 일어날 수 있다는 점이다. 이러한 반응 분리는 황화광물 표면의 피막(passivation) 형성을 억제하고, 전자 전달 경로를 안정적으로 유지함으로써 금속 침출 효율과 전력 생산의 연속성을 동시에 향상시켰다.
실험 결과, 최대 전력밀도는 5.4 mW/m2로 나타났고, 10일간의 운전 동안 납 37.3 mg/kg, 아연 84.2 mg/kg이 침출되어 각각 1.4%와 0.6%의 침출율을 기록하였다. 이를 연간 추출율로 환산하면 납은 약 50%/year, 아연은 약 20%/year로 계산되어, 기존의 힙리칭(heap leaching) 공정에서 보고된 침출 효율과 유사한 수준을 보였다. 이러한 결과는 연료전지 기반 시스템이 화학적 혹은 미생물 기반 침출 공정과 비교해도 경쟁력 있는 금속 회수 성능을 확보하고 있음을 의미한다. 또한 현장 적용 시나리오 평가 결과, 1 m2 모듈(20 × 20 unit cells)은 약 6.0 mW(2 V)의 전력을 생산하였으며, 이를 20,900 m2 규모의 광미 적치장에 적용할 경우 약 125 W의 전력 생산이 가능할 것으로 산정되었다. 이는 LED 조명 및 저전력 센서를 외부 전원 없이 구동할 수 있는 수준으로, 연료전지가 광미 처리 현장에서 자가발전형 금속 회수 장치로서 기능할 수 있음을 시사한다.
따라서, 본 연구에서 제안한 연료전지 기반 침출 시스템은 광미 내 황화광물의 지속적인 산화 반응을 전기화학적으로 유도하여, 금속 회수와 전기 생산을 동시에 달성할 수 있는 에너지 자립형 자원 회수 기술로 평가된다. 이는 향후 광산 폐기물의 환경 저감 및 유용 금속의 순환자원화에 기여할 수 있는 지속가능한 기술적 대안으로서의 잠재력을 보여준다.
본 연구는 환경부의 재원으로 한국환경산업기술원의 지중환경오염∙위해관리기술개발사업의 지원을 받아 연구되었습니다(RS-2018-KE000140). 또한, 서울대학교 공학연구원의 기술적 지원에도 감사드립니다.
- 1. Aikawa, K., Ito, M., Segawa, T., Jeon, S., Park, I., Tabelin, C.B., and Hiroyoshi, N., 2020, Depression of lead-activated sphalerite by pyrite via galvanic interactions: Implications to the selective flotation of complex sulfide ores. Minerals Engineering, 152, 106367.
-

- 2. Adiansyah, J.S., Rosano, M., Vink, S., and Keir, G., 2015, A framework for a sustainable approach to mine tailings management. Journal of Cleaner Production, 108, 1050-1062.
-

- 3. Chen, J., Liu, J., Hu, M., Liu, J., Yu, Y., Zhou, Y., Bao, N., Han, X., and Guo, F., 2024, Potential and characteristics of heavy metals electrokinetic removal from the copper-zinc mine tailings: Study on the simulated and actual tailings. Chemical Engineering Journal, 496, 154245.
-

- 4. Chopard, A., Plante, B., Benzaazoua, M., Bouzahzah, H., and Marion, P., 2017, Geochemical investigation of the galvanic effects during oxidation of pyrite and base-metals sulfides. Chemosphere, 166, 281-291.
-

- 5. Ge, X., Cao, X., Song, X., Wang, Y., Si, Z., Zhao, Y., Wang, W., and Tesfahunegn, A.A., 2020, Bioenergy generation and simultaneous nitrate and phosphorus removal in a pyrite-based constructed wetland-microbial fuel cell. Bioresource Technology, 296, 122350.
-

- 6. Hussaini, S., Tita, A.M., Kursunoglu, S., Top, S., Ichlas, Z.T., Kar, U., and Kaya, M., 2021, Pb-Zn recovery from a malic leach solution of a carbonate type ore flotation tailing by precipitation and solvent extraction. Separation and Purification Technology, 272, 118963.
-

- 7. Ju, W.J., Jho, E.H., and Nam, K., 2018, Effect of initial pH, operating temperature, and dissolved oxygen concentrations on performance of pyrite-fuel cells in the presence of Acidithiobacillus ferrooxidans. Journal of Hazardous Materials, 360, 512-519.
-

- 8. Ju, W.J., Jho, E.H., and Nam, K., 2025, Facilitation of pyrite dissolution through enhanced electron transfer in pyrite-fuel cells. Journal of Hazardous Materials, 490, 137788.
-

- 9. Khalil, A., Ait-Khouia, Y., Beniddar, H., El Ghorfi, M., Hakkou, R., Taha, Y., and Benzaazoua, M., 2025, Sustainable reprocessing of Pb-Zn mine tailings through froth flotation for resource recovery and environmental remediation in abandoned mining regions. Minerals Engineering, 222, 109132.
-

- 10. Kim, K., 2024, Global trends and implications of critical mineral supply chains [in Korean]. KIEP World Economy Brief, 24-4 Current Issue 1, Korea Institute for International Economic Policy (KIEP), Sejong, Korea.
- 11. KMOE, 2014a, 폐기물 공정시험기준 [in Korean]. Ministry of Environment, Sejong, Korea.
- 12. Li, Y., Kawashima, N., Li, J., Chandra, A.P., and Gerson, A.R., 2013, A review of the structure, and fundamental mechanisms and kinetics of the leaching of chalcopyrite. Advances in Colloid and Interface Science, 197, 1-32.
-

- 13. Lizama, H.M., Harlamovs, J.R., Belanger, S., and Brienne, S.H., 2003, The Teck Cominco Hydrozinc¢â process. Electrometallurgy and Environmental Hydrometallurgy, 2, 1503-1516.
-

- 14. Mudd, G.M., Jowitt, S.M., and Werner, T.T., 2017, The world's lead-zinc mineral resources: Scarcity, data, issues and opportunities. Ore Geology Reviews, 80, 1160-1190.
-

- 15. Park, I., Tabelin, C.B., Jeon, S., Li, X., Seno, K., Ito, M., and Hiroyoshi, N., 2019, A review of recent strategies for acid mine drainage prevention and mine tailings recycling. Chemosphere, 219, 588-606.
-

- 16. Qian, G., Fan, R., Short, M.D., Schumann, R.C., Li, J., Smart, R.St.C., and Gerson, A.R., 2018, The effects of galvanic interactions with pyrite on the generation of acid and metalliferous drainage. Environmental Science & Technology, 52(9), 5349-5357.
-

- 17. Rouchalova, D., Rouchalova, K., Janakova, I., Cablik, V., and Janstova, S., 2020, Bioleaching of iron, copper, lead, and zinc from the sludge mining sediment at different particle sizes, pH, and pulp density using Acidithiobacillus ferrooxidans. Minerals, 10(11), 1013.
-

- 18. USGS, 2018, Mineral Commodity Summaries 2018. U.S. Geological Survey, Reston, VA.
- 19. USGS, 2024, Mineral Commodity Summaries 2024. U.S. Geological Survey, Reston, VA.
- 20. USEPA, 1992, Method 1311: Toxicity Characteristic Leaching Procedure (TCLP). U.S. Environmental Protection Agency, Office of Solid Waste and Emergency Response, Washington, DC.
- 21. USEPA, 1996, Method 3052: Microwave assisted acid digestion of siliceous and organically based matrices. U.S. Environmental Protection Agency, Office of Research and Development, Washington, DC.
- 22. Viollier, E., Inglett, P.W., Hunter, K., Roychoudhury, A.N., and Van Cappellen, P., 2000, The ferrozine method revisited: Fe(II)/Fe(III) determination in natural waters. Applied Geochemistry, 15(6), 785-790.
-

- 23. Yan, J., Hu, X., He, Q., Qin, H., Yi, D., Lv, D., Cheng, C., Zhao, Y., and Chen, Y., 2021, Simultaneous enhancement of treatment performance and energy recovery using pyrite as anodic filling material in constructed wetland coupled with microbial fuel cells. Water Research, 201, 117333.
-

- 24. Yang, J.-S., Lee, J.Y., Baek, K., Kwon, T.-S., and Choi, J., 2009, Extraction behavior of As, Pb, and Zn from mine tailings with acid and base solutions. Journal of Hazardous Materials, 171(1-3), 443-451.
-

- 25. Ye, M., Li, G., Yan, P., Ren, J., Zheng, L., Han, D., Sun, S., Huang, S., and Zhong, Y., 2017, Removal of metals from lead-zinc mine tailings using bioleaching and followed by sulfide precipitation. Chemosphere, 185, 1189-1196.
-

 This Article
This Article
-
2025; 30(6): 55-62
Published on Dec 31, 2025
- 10.7857/JSGE.2025.30.6.055
- Received on Oct 2, 2025
- Revised on Oct 17, 2025
- Accepted on Oct 22, 2025
 Services
Services
Shared
 Correspondence to
Correspondence to
- Kyoungphile Nam
-
Department of Civil and Environmental Engineering, Seoul National University, Seoul 08826, Korea
- E-mail: kpnam@snu.ac.kr





