- Immobilization of Hexavalent Chromium Through Reductive Zones Generated by Fe-bearing Clay Mineral Acting as an Electron Mediator
Changyu Moon1, Sang Hyun Kim2, Jaeshik Chung2, and Kyoungphile Nam1*
1Department of Civil and Environmental Engineering, Seoul National University, Seoul 08826, South Korea
2Water Cycle Research Center, Korea Institute of Science and Technology (KIST), Seoul 02792, South Korea- 철 함유 점토광물의 전자 매개를 이용한 환원구역 생성과 이를 통한 6가 크롬의 고정화
문찬규1ㆍ김상현2ㆍ정재식2ㆍ남경필1*
1서울대학교 건설환경공학부, 2한국과학기술연구원 물자원순환연구단
This article is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
This study evaluated the potential of montmorillonite as a reactive medium for Cr(VI) remediation through dithionite-mediated reduction of structural Fe(III) to Fe(II). Batch experiments revealed that dithionite treatment generated up to 19.1 mg/g Fe(II), representing 83% of total structural iron (23 mg/g). The reduction behavior was governed by redox potential equilibrium rather than reductant concentration. The generated Fe(II) effectively reduced Cr(VI) following a 3:1 stoichiometry, with all Fe(II) quantitatively consumed for Cr(VI) removal. Solid-phase analysis using SEM-EDS and XPS confirmed that reduced Cr(III) was immobilized as Cr(OH)3 on clay surfaces, with no aqueous total chromium detected. In the column experiments, a 2 PV pulse injection of 50 mM dithionite lowered the ORP to -200 mV and generated structural Fe(II) within the medium. Following dithionite flushing, continuous injection of Cr(VI) solution exhibited delayed breakthrough up to 10 PV, indicating that the structural Fe(II) within the solid matrix served as an electron donor for Cr(VI) reduction. Sectional analysis and EPMA mapping confirmed immobilized Cr associated with montmorillonite particles. Dithionite reinjection successfully regenerated the reductive zone and restored the Cr(VI) removal capacity, thereby extending the operational lifetime of the reactive medium.
Keywords: Hexavalent chromium, Fe-bearing montmorillonite, Structural Fe(II), In situ reductive zone
다양한 산업으로 방출된 6가 크롬(Cr(VI))은 제련, 전기도금, 피혁 가공 등 여러 산업활동에서 기인하며, 지하수에서 흔히 발견되는 독성 오염물질이다 (Guo et al., 2024). 수중에서 Cr(VI)는 주로 CrO42-, Cr2O32-와 같은 산소음이온(oxyanion) 형태로 존재하며, 이는 용해도가 높고 이동성이 크며 광물 표면에 대한 흡착 친화력이 낮아 수자원에 장기적인 위해를 초래한다(Richard & Bourg, 1991). Cr(VI)의 장기 노출은 호흡기 질환, 신장 및 간 손상, 암 발생 위험 증가와 같은 심각한 건강 피해와 연관되어 있는 것으로 보고되었다(DesMarias & Costa, 2019). 이에 따라 다수의 규제 기관에서는 음용수 내 Cr(VI) 농도 기준을 50 μg/L 이하로 엄격히 제한하고 있다.
Cr(VI)는 산화환원 조건에 따라 화학적 종이 결정되는 전형적인 산화환원 민감성 오염물질(redox-sensitive conta- minant)로 알려져 있다(Richard & Bourg, 1991). 혐기성 조건에서 Cr(VI)는 Cr(III)로 환원되며, Cr(III)는 Cr(VI)와 달리 독성이 거의 없고 상대적으로 낮은 이동성을 보인다. 이는 Cr(III)가 광물 표면이나 유기물에 쉽게 흡착되고, 중성 및 알칼리성 조건에서는 침전되기 때문이다. 따라서 Cr(VI)를 Cr(III)로 환원시키는 과정은 크롬 오염 정화의 핵심 접근법으로 여겨진다(Zulfiqar et al., 2023).
현장 산화환원 조절법(In situ Redox Manipulation, ISRM)은 산화환원 민감성 오염물질의 지하수 정화에 있어 유망한 기술로 평가받고 있다(Vermeul et al., 2003). ISRM은 환원제를 대수층에 주입하여 투수성 환원 구역을 형성한 뒤, 환원 구역을 통과하는 오염물질을 저독성·저이동성 형태로 전환시키는 방식이다(Istok et al., 1999). 일단 환원 구역이 형성되면, 지하수 유동에 따라 이동하는 오염물질이 지속적으로 처리될 수 있다. 이러한 ISRM은 광범위하게 분산된 오염 plume이나 심부 오염과 같이 굴착 또는 pump-and-treat 방법의 적용이 어려운 부지에서 유용하다(Fruchter et al., 1996). 황철석, 녹슨광(green rust), 자철석(magnetite), 흑운모(biotite), 철 함유 점토광물 등 다양한 대수층 매질이 활용될 수 있으며, 그 성능은 매질의 환원 능력과 산화환원 안정성에 의해 결정된다(Boparai et al., 2008).
그러나, 기존에 주로 활용된 녹슨광, 자철석, 흑운모 등은 높은 초기 환원 능력을 가지나, 오염물질과의 반응 과정에서 광물 표면에 Fe-Cr 복합체와 같은 passivation layer가 형성되어 반응 효율이 저하되고, 환원 환경에서 reductive dissolution에 의해 Fe(II)가 수용액으로 용출될 수 있는 우려가 있다(He & Traina, 2005; Ribeta et al., 1995). 반면 철을 함유한 점토광물은 지하환경에서 흔히 존재하고, 산화환원 반응에서 안정적으로 작용할 수 있으며, Cr(VI)과 같은 산화환원 민감성 오염물질과 직접적으로 반응할 수 있다는 점에서 최근 주목받고 있다(Ilgen et al., 2019).
점토광물의 구조철(structural Fe)은 팔면체층에서 Al3+과 동형치환(isomorphous substitution)을 통해 최대 30 wt%까지 존재하며, 환경 조건에 따라 Fe(III)와 Fe(II) 사이를 가역적으로 순환한다(Neumann et al., 2011). 일반적인 산화 조건에서 구조철은 Fe(III)로 존재하지만, dithionite와 같은 환원제 처리 시 Fe(II)로 환원되며, Cr(VI)를 Cr(III)로 전환하는 전자공여체로 작용한다(Joe-Wong et al., 2017). 또한, 소모된 Fe(II)는 dithionite의 재주입을 통해 재생될 수 있어 환원 구역의 성능 회복이 가능할 것으로 제시되고 있다(Yu et al., 2024).
구조철의 산화환원 거동에 대해서는 다수의 연구가 진행되어 왔다. 2000년대 후반까지는 구조철의 환원 거동과 이에 따른 구조적·물리적 변화 및 환원 메커니즘 규명에 집중되었으며(Neumann et al., 2011; Komadel et al., 2006; Stucki et al., 1996), 이후에는 Fe(II)를 포함한 점토광물이 Cr(VI), U(VI), Tc(VI), PCE, TCE 등 다양한 오염물질을 환원시키는 가능성이 연구되었다(Joe-Wong et al., 2017; Tsarev et al., 2016). 그러나 구조철 기반 점토광물의 환원능력, 이를 이용한 Cr(VI) 고정화 메커니즘에 대한 이해는 여전히 제한적이며, 환원능력의 재생 가능성이 제시되었음에도 불구하고 이에 대한 실질적인 평가는 이루어지지 않았다. 특히 유동 조건에서 환원 구역의 형성 및 정화능력, 장기운전 가능성에 대한 평가는 충분히 이루어지지 않았다.
따라서 본 연구는 철 함유 점토광물을 활용한 Cr(VI)의 현장 고정화 기술을 다루며, 다음의 세부 목표를 설정하였다. 첫째, dithionite 처리에 따른 구조철 Fe(II) 생성량 규명과 Cr(VI) 제거 능력 평가, 둘째, 분광학적 분석을 통한 환원 메커니즘과 Cr(III) 고정화 형태 규명, 셋째, dithionite 재주입에 따른 구조철 재생성과 장기 안정성 검토, 넷째, 컬럼 실험을 통한 유동 조건에서의 환원 구역 형성 및 회복 가능성 확인이다
2.1. 재료
본 연구에 사용된 점토광물은 Clay Mineral Society (https://www.clays.org)로부터 구입한 montmorillonite(SWy-3)이다. 전처리 과정은 Moon et al.(2025)의 방법을 따랐다. 시료를 1 M NaCl 용액에 24시간 침지하여 나트륨 포화(sodium saturation)시킨 후, 탈이온수로 3회 세척하였다. 이후 현탁액을 HNO3로 pH 3까지 조정하고 1시간 교반하여 calcite 및 iron oxyhydroxide를 용해시키고, 약하게 흡착된 Fe(III)를 제거하였다(Gorski et al., 2013). 이후 원심분리(12,000 g, 10분)를 하여 상등액을 제거하고 침전물을 증류수에 재현탁하였다. 시료는 40oC에서 건조 후 분쇄하여 63 μm 이하(<230 mesh)의 분말을 확보하였다. 전처리된 montmorillonite를 하단에서 서술할 점토광물 용해 및 1,10-phenanthroline 방법을 통해 분석한 결과, 전체 구조철 함량은 2.3 wt%이며 모두 Fe(III) 상태로 존재하는 것으로 확인되었다.
2.2. Dithionite를 이용한 montmorillonite 내 구조철 환원 실험
Montmorillonite 내 구조철 Fe(III)의 화학적 환원은 dithionite를 사용하여 수행하였다. 전처리된 montmorillonite 100 mg을 50 mL 세럼병에 넣고, 5, 10, 50, 100, 200 mM 농도의 dithionite 용액(탄산염 완충용액, pH 9) 40 mL를 각각 주입하였다. 세럼병은 부틸 고무 마개와 알루미늄 캡으로 밀봉한 뒤 실온(25 ± 1oC)에서 최대 96시간 동안 반응시켰다. 환원 처리된 montmorillonite는 원심분리로 회수한 뒤, 잔류 dithionite를 제거하기 위해 탈산소 증류수로 3회 세척하였다. 환원된 시료는 전 실험 기간 동안 혐기성 챔버에서 보관하였으며, 보관 중 주기적으로 시료를 채취하여 용해한 후 1,10-phenanthroline 방법으로 Fe(II) 함량을 측정하여, Fe(II)/total Fe 비율은 안정적으로 유지됨을 확인하였다. 각 조건은 동일하게 3회 반복하여 수행하였다.
2.3. 환원된 구조철 함유 montmorillonite를 이용한 Cr(VI) 제거 실험
제조된 Fe(II) 함유 점토광물의 6가 크롬 제거 능력을 확인하기 위해 배치 실험을 진행하였다. 50 mM dithionite로 환원 처리한 montmorillonite(1.54 wt% Fe(II))와 환원되지 않은 montmorillonite를 크롬 용액과 반응시켰다. K2CrO4를 HEPES buffer(pH 7)에 용해하여 10 mg/L Cr(VI) 용액 40 mL를 세럼병에 분취하고, montmorillonite 100 mg(고액비 2.5 g/L)을 첨가한 후 밀봉하였다. 모든 실험은 대기 중 산소에 의한 산화를 방지하기 위해 혐기성 챔버 내에서 수행하였으며, 상온에서 교반(150 rpm)하며 500시간까지 반응시켰다. 각 조건은 동일하게 4회 반복하여 수행하였다. 특정 시점에 시료를 채취하여 0.45 μm 시린지 필터로 여과한 후, 여과액의 Cr(VI) 및 총 크롬 농도를 측정하였다. 또한, 환원된 montmorillonite의 단위 질량당 Cr(VI) 제거 용량을 평가하기 위해 고액비를 0.1, 0.5, 1, 2, 5 g/L로 변화시키며 동일한 조건에서 수행하였다.
구조철 Fe(II)의 Cr(VI) 제거에 대한 재사용성을 평가하기 위해 산화환원 반복 실험을 수행하였다. 앞선 실험에서 Cr(VI) 제거 반응에 사용한 시료를 회수하여, 40 mL의 50 mM dithionite 로 재처리하여 Fe(II)를 재생시켰다. 이후 잔류 dithionite를 제거하기 위해 질소로 퍼지한 증류수로 3회 세척한 뒤 다시 Cr(VI)와 반응시켰다. 이러한 재생 사이클은 총 4회 반복하였으며, 각 사이클 종료 시 하나의 시료를 회수하여 구조철 Fe(II)와 총 철 함량을 분석하였다.
2.4. 컬럼 실험
컬럼 실험은 내경 8.0 cm, 길이 8.0 cm의 아크릴 컬럼을 사용하여 수행하였다. 주문진사와 montmorillonite 혼합물(95:5 wt%)을 균질하게 혼합한 후 세 개의 독립된 컬럼에 각각 충진하였으며, 충진된 컬럼의 유효 공극률은 약 0.33으로 계산되었다. 각 컬럼은 질소로 퍼지한 증류수를 10 pore volume(PV) 이상 흘려 안정화 과정을 거친 후 실험에 사용하였다. 유입 용액은 peristaltic pump를 이용하여 상향류 조건에서 0.4 mL/min의 유량으로 주입하였다.
컬럼 실험에 사용한 모든 용액은 질소로 퍼지하여 혐기 조건을 유지하며 진행하였다. 구조철의 환원은 50 mM dithionite 용액(pH 9)을 2 PV 동안 pulse 주입하여 수행하였으며, 주입 후 질소 퍼징 증류수로 전환하여 잔류 dithionite를 제거하였다. 이 과정에서 배출되는 유출수를 채취하여 dithionite 농도와 oxidation-reduction potential(ORP)를 측정하였다. 이후 유입 용액을 50 mg/L Cr(VI) 용액으로 전환하여 파과곡선을 도출하였으며, KBr tracer 실험 결과와 비교하였다. Dithionite 환원 직후와 Cr(VI) 주입실험 완료 후 각각 컬럼을 해체하여 높이별(2, 4, 6, 8 cm)로 시료를 채취하였으며, 각 시료의 Fe(II) 함량 및 고정화된 Cr 함량을 측정하였다.
또한, 환원 구역의 재생 가능성을 평가하기 위해 별도의 컬럼에서 dithionite 재주입 실험을 수행하였다. 상기 방법과 동일하게 dithionite pulse 주입과 Cr(VI) 연속 주입을 총 4회 반복하여 환원 구역의 재생성을 평가하였다.
2.5. 분석 방법
Cr(VI) 농도는 diphenylcarbazide(DPC) 방법을 적용하여, 540 nm에서 UV-Vis spectrophotometer를 이용한 비색법으로 측정하였다. 총 크롬 농도는 유도결합플라즈마 분광기(ICP-OES, iCAP 7000 series, Thermo Fisher Scientific)를 이용하여 분석하였으며, 수용액 내 Cr(III) 농도는 총 크롬 농도에서 Cr(VI) 농도를 차감하여 계산하였다. 이는 수중 크롬이 Cr(VI)와 Cr(III) 형태로만 존재한다고 가정한 것이다(Wójcik et al., 2020).
점토광물의 구조철 함량은 변형된 1,10-phenanthroline 방법을 이용하여 측정하였다(Amonette and Templeton, 1998). 반응이 끝난 시료를 회수한 후, 90°C 이상에서 가열하여 탈기(degassed)한 혼합산(8% HF 및 10% H2SO4)과 반응시켜 완전히 용해시켰다. 시료의 완전한 용해를 확인한 후, 용액 중 Fe(II) 농도를 1,10-phenanthroline 착화반응으로 정량하였다. 총 철(total Fe) 함량은 시료 용액에 hydroxylamine sulfate(NH2OH·H2SO4)를 첨가하여 모든 철을 2가 상태로 환원시킨 후, 동일한 방법으로 측정하였다. Fe(II) 및 Fe(III) 표준용액(ammonium ferrous sulfate hexahydrate, ferric sulfate)을 이용한 검증 실험을 통해 용해 과정 중 추가적인 산화·환원이 발생하지 않음을 확인하였다.
환원 실험 후 시료의 고형상 분석을 위해 혐기 조건에서 건조 후 FE-SEM-EDS (Zeiss, Germany), EPMA (JEOL, Japan), XPS (Thermo Fisher, UK)를 이용하였다. FE-SEM-EDS와 EPMA로 표면 형태 및 Cr 분포를 관찰하였으며, XPS Cr 2p 스펙트럼을 통해 Cr 화학종을 규명하였다. XPS 데이터는 CasaXPS (v2.3.25)로 처리하였다.
3.1. Dithionite 처리로 생성 가능한 montmorillonite 내 구조철 Fe(II) 함량
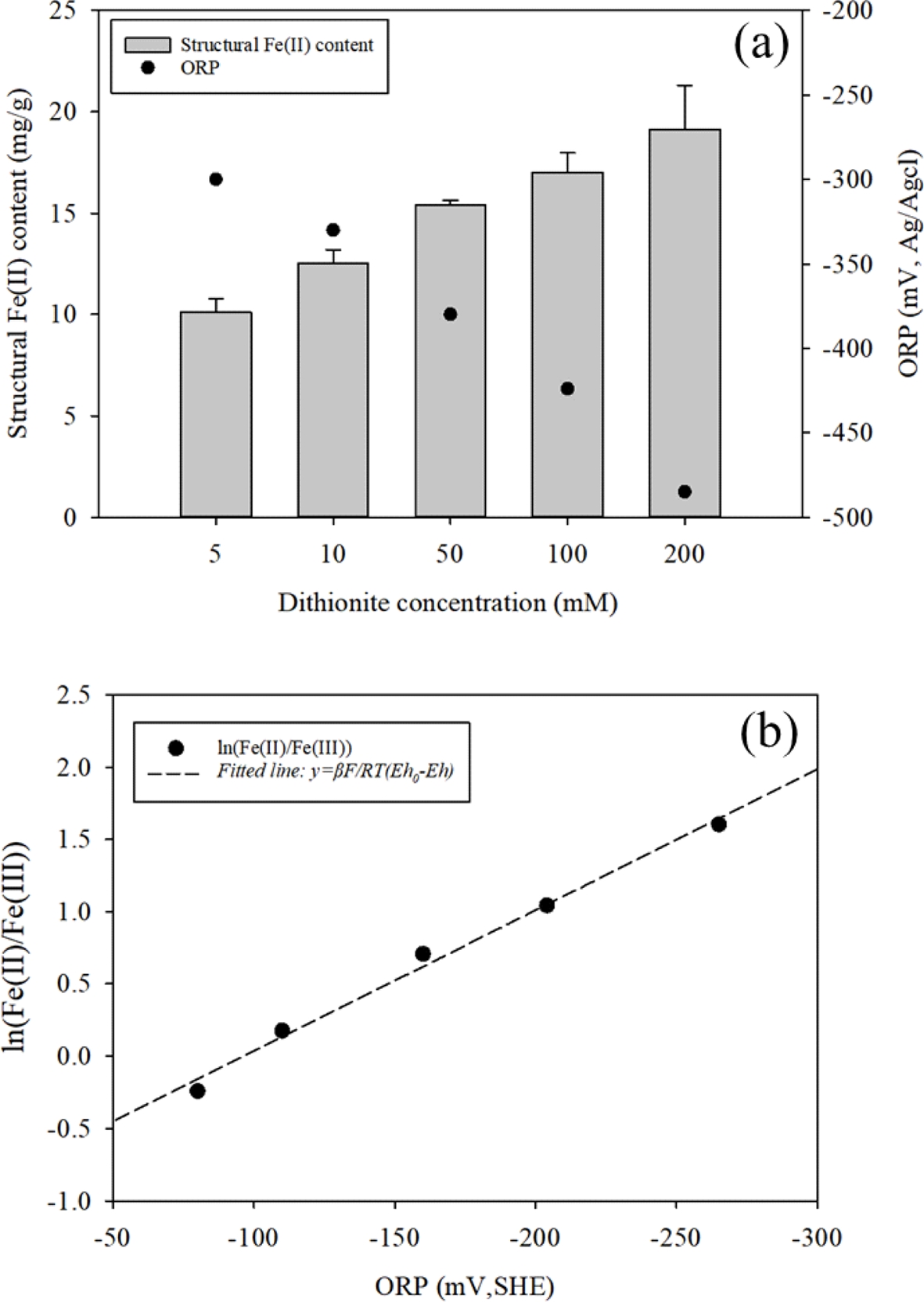
본 실험은 dithionite 처리에 의해 생성될 수 있는 구조철 Fe(II) 함량을 확인하기 위해 수행되었다. Fig. 1(a)는 dithionite 처리 농도에 따른 montmorillonite 내 구조철 환원량을 보여준다. Dithionite 농도가 증가함에 따라 Fe(II) 생성량은 점차적으로 증가하여 최대 약 19.1 mg/g까지 도달하였다. 그러나 점토 내 총 구조철 함량이 약 23 mg/g임을 고려할 때, 충분한 반응 시간과 과량의 dithionite가 잔존함에도 불구하고 실제 환원된 Fe(II)는 구조철 전체의 일부에 국한되었다. 이는 구조철이 환원제 농도에 단순히 비례하여 전부 환원되지 않으며, 산화환원전위(redox potential)에 의해 평형 수준이 결정되기 때문으로 해석된다(Gorski et al., 2013; Neumann et al., 2011).
각 조건에서 측정한 구조철 내 Fe(II)/Fe(III) 비를 Nernst 식에 기반한 선형식(식 (1))으로 회귀분석하였다.

여기서 Eh0는 구조철의 표준 산화환원전위, Eh는 측정 산화환원전위, β는 구조철 특성 계수(Gorski et al., 2013), R은 기체상수(8.314 J/mol·K), T는 절대온도(K), F는 Faraday 상수(96485 C/mol)이다.
그 결과, 구조철 내 ln[Fe(II)/Fe(III)] 비는 (Eh-Eh0)와 명확한 선형 관계를 보였으며, 이를 통해 산출된 montmorillonite의 표준 산화환원전위(Eh0)는 약 -160 mV(SHE) 였다(Fig. 1(b)). Montmorillonite의 구조철은 팔면체층 내에 고정되어 있어 수용액상의 Fe2+/Fe3+ 이온과는 상이한 산화환원 평형 조건을 갖는다(Stucki et al., 1996; Komadel et al., 2006; Neumann et al., 2011). 결정학적 제약과 배위환경으로 인해 구조철은 고유의 표준 산화환원전위를 나타내며, 광물의 종류와 구조적 특성에 따라 다른 값을 갖는다(Gorski et al., 2013). 본 연구에서 구한 약 -160 mV(SHE)의 값은 구조철의 특성을 반영하며, 기존 문헌에서 보고된 montmorillonite의 전위 범위와 일치하였다.
3.2. 구조철 환원에 의한 Cr(VI) 제거 및 고정화
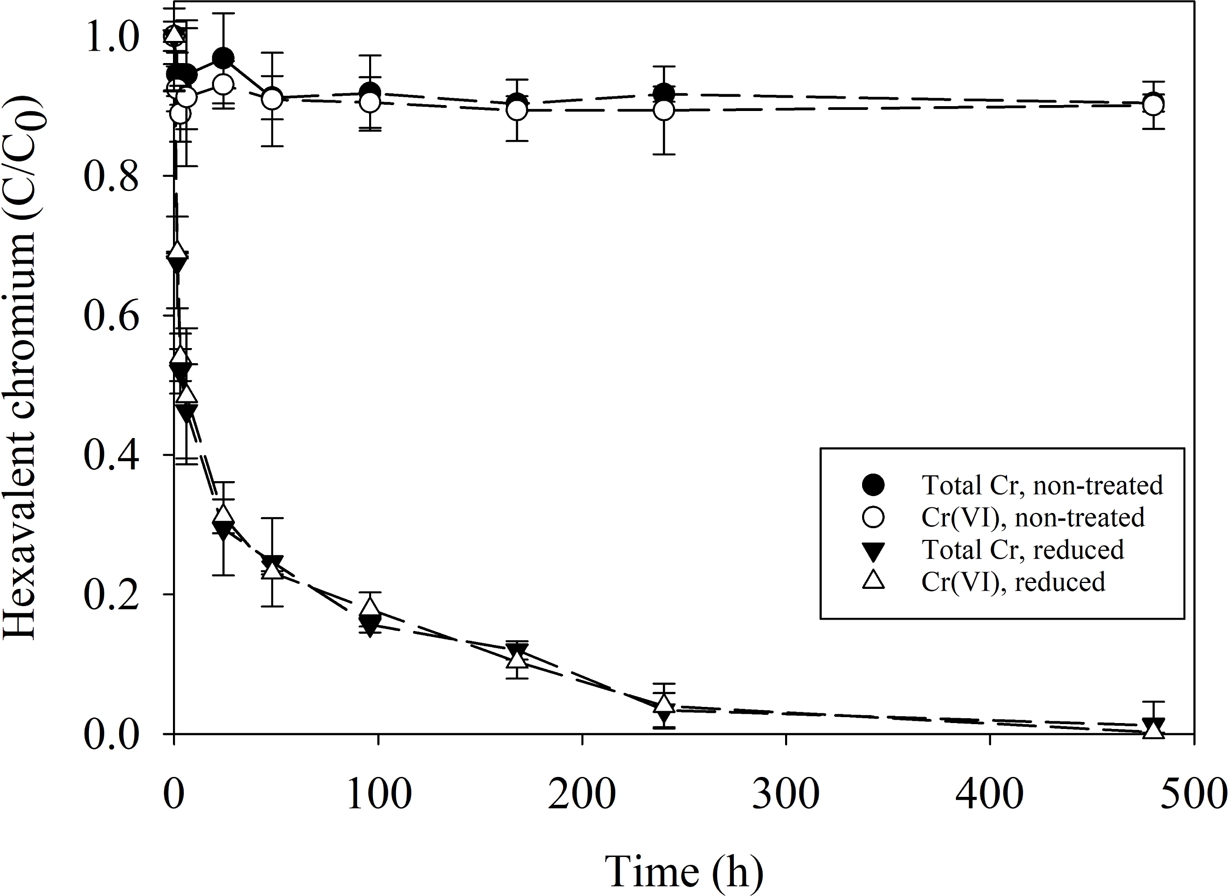
Fig. 2는 환원처리된 montmorillonite와 비환원 시료의 Cr(VI) 제거를 시간에 따라 나타낸 것이다. 비환원된 montmorillonite의 경우, 소폭 감소하였으나(최대 9%), 전체적으로는 반응 시간 전반에 걸쳐 미미한 변화만을 보였다. 이러한 미미한 제거는 Cr(VI)가 HCrO4-와 같은 음이온으로 존재하고 montmorillonite 표면도 음전하를 띠어, 정전기적 반발로 인해 제한적인 흡착만 일어났기 때문으로 판단된다(Guerra et al., 2014). 이와 대조적으로, dithionite로 환원 처리한 montmorillonite는 반응 초기부터 Cr(VI)를 급격히 제거하여 최종적으로 검출 한계 이하로 감소시켰다. 이는 구조철의 Fe(II)가 Cr(VI)를 Cr(III)로 환원하는 산화환원 반응에 기인한다. 주목할 점은 총 크롬 농도 역시 Cr(VI)와 거의 동일하게 감소하였는데, 이는 환원된 Cr(III)가 용액에 남아있지 않고 점토 표면 흡착 또는 Cr(OH)3 침전을 통해 고정화되었음을 의미한다.
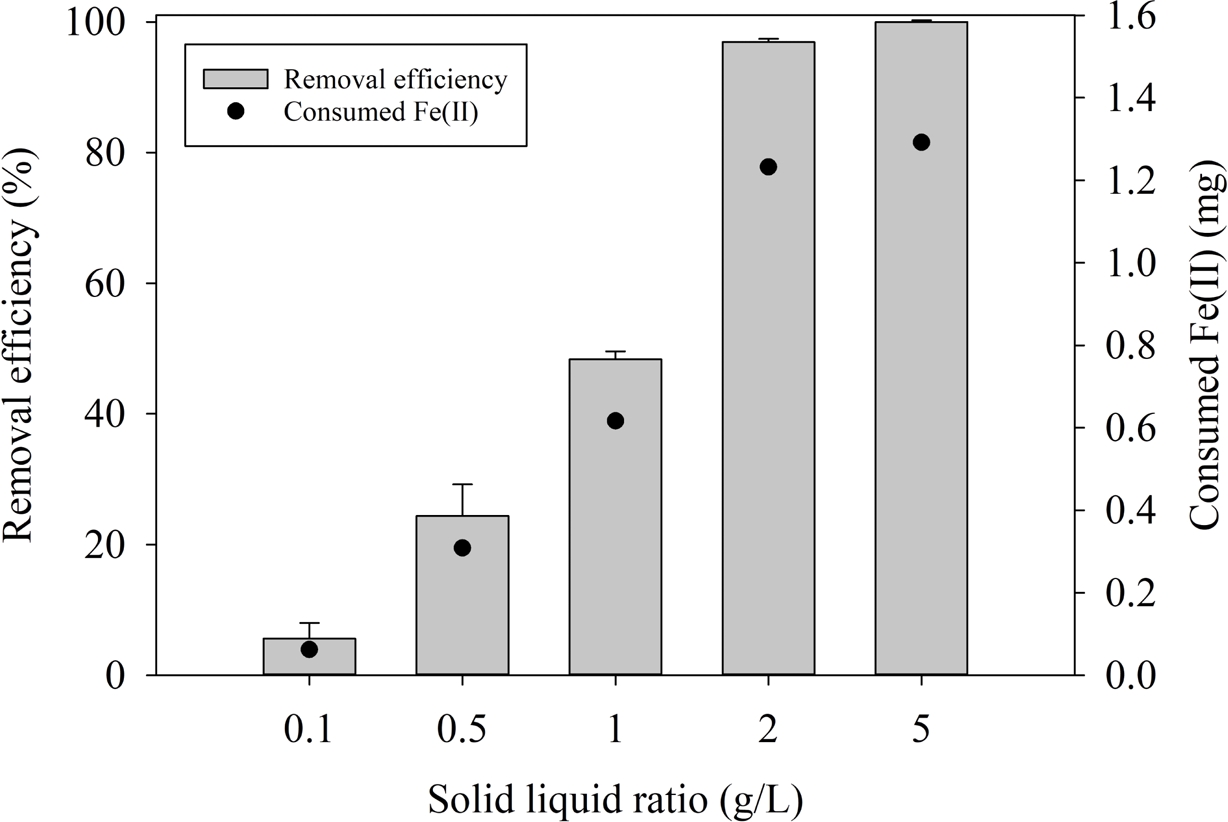
Montmorillonite의 크롬 제거 용량을 확인하기 위해 고액비 변화에 따른 Cr(VI) 제거 특성을 평가한 결과를 Fig. 3에 나타내었다. 고액비가 0.1 g/L에서 5.0 g/L로 증가함에 따라 Cr(VI) 제거 효율은 약 5%에서 100%로 증가하였다. 특히 고액비 2.0 g/L 이상에서는 거의 완전한 제거(>95%)가 달성되었다. 반응 종료 후 매질을 수거하여, 잔류 Fe(II)를 측정하여 소모된 Fe(II) 양을 계산하였다. 고액비 0.1~2.0 g/L 조건에서는 투입된 Fe(II)가 거의 모두 소모되었으며, 고액비 5 g/L에서는 약 42%의 Fe(II)가 소모되었다. 이는 화학양론적 비율(Fe(II):Cr(VI) = 3:1)과 일치하는 결과로, dithionite 환원을 통해 생성된 구조철 Fe(II)는 Cr(VI) 제거에 정량적으로 이용 가능하며, 이론적 제거 용량(4.77 mg Cr(VI)/g montmorillonite)을 달성할 수 있음을 확인하였다.
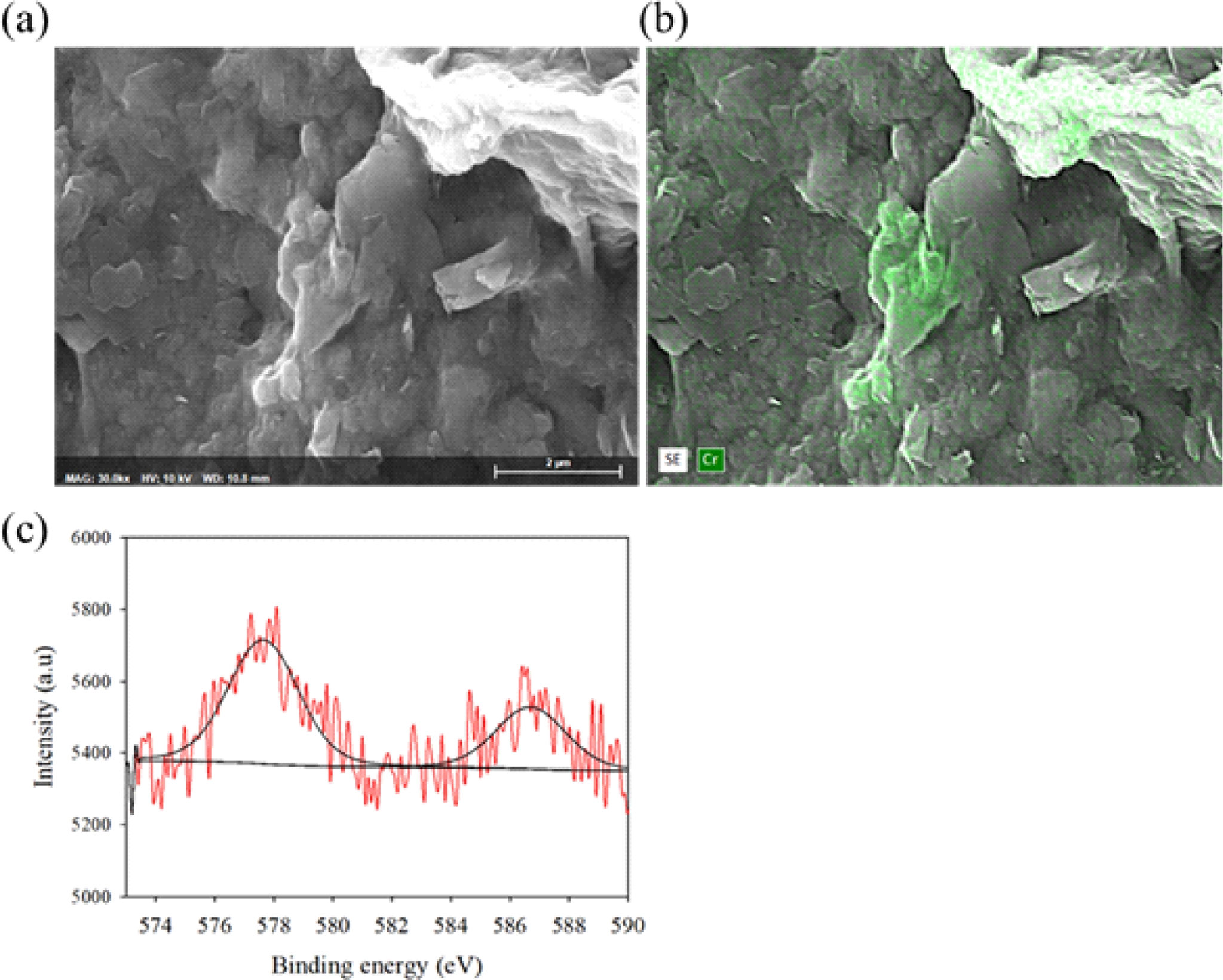
제거된 Cr(III)의 고정화 기작을 규명하기 위해, SEM-EDS 및 XPS 분석을 수행하였다(Fig. 4). Fig. 4(a)와 4(b)의 SEM 관찰과 원소 매핑에서 점토 표면에 크롬이 농축된 입자상 침전물이 국소적으로 분포하는 것이 확인되었다. XPS 분석 결과 고형 시료 내 크롬은 모두 3가 상태로 존재하는 것으로 확인되었다. Fig. 4(c)에서 Cr 2p3/2 피크는 577.0–578.5 eV 범위에서 나타났으며, 이는 Cr(III) 산화 상태에 해당한다(Biesinger et al., 2004). 관찰된 결합에너지(577.6 eV)는 환원된 크롬이 주로 montmorillonite와 결합된 Cr(OH)3 형태로 존재함을 보여준다.
실험에서 얻은 농도–시간 곡선을 이용하여 반감기를 추정하였다. 초기 구간에서의 반감기는 약 4시간으로 계산되었으며, 이에 대응하는 유사 일차 속도상수는 0.171 h-1로 산정되었다. 용액상 Fe(II)의 유효농도를 고려한 이차 속도상수는 0.249 mM-1 h-1로 계산되었다. 이 값은 Cr(VI)을 환원하는 다른 환원제에서 보고된 속도상수, 즉 이가철 이온, 영가철, mackinawite, green rust 등에서 제시된 범위(1–100 mM-1 h-1)에 비해 낮은 수준에 해당한다(Buerge & Hug, 1997; Du et al., 2016; Mullet et al., 2004; Williams & Scherer, 2001). 이러한 차이는 구조철 Fe(II)가 점토 격자 내에 고정되어 있어 전자전달이 주로 표면 반응에 국한되기 때문으로 판단된다. 따라서 Fe(II)-bearing 점토광물을 이용한 Cr(VI) 제거에는 충분한 반응시간이 필요하며, 점토광물이 포함된 환원 구역을 적용할 때에는 체류시간이 제한된 유동 조건에서도 제거 효율이 유지되는지를 규명할 필요가 있음을 시사한다.
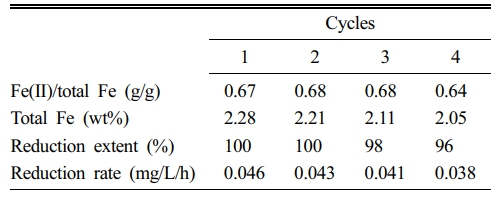
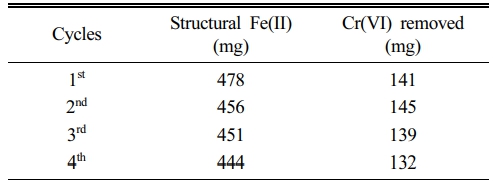
반응이 종료된 montmorillonite를 회수하여 50 mM dithionite로 다시 환원시킨 후 Cr(VI) 환원 실험을 반복 수행하였다. Table 1에 나타난 바와 같이, 4회 재생 사이클 동안 Fe(II)/total Fe 비율은 0.64–0.68 수준으로 안정적으로 유지되었으며, 이는 동일한 환원 조건에서 구조철이 반복적으로 Fe(II) 상태로 재생되었음을 의미한다. 한편, 총 철 함량은 반복 사용 과정에서 2.28 wt%에서 2.05 wt%로 약 10% 감소하였으며, dithionite 처리 과정에서 점토의 층상구조 일부가 해리되며 구조철이 용출된 결과로 판단된다(Moon et al., 2025). 그 결과, Cr(VI) 제거율은 100%에서 96%로, 제거 속도는 0.046 mg/L/h에서 0.038 mg/L/h로 점차 감소하였다. 그러나 4회 반복 후에도 96% 이상의 높은 제거 효율을 유지하여, 구조철이 dithionite 재주입을 통해 반복적으로 재생 가능하며, Cr(VI)의 제거가 가능함을 확인하였다.
3.3. Dithionite 주입에 따른 montmorillonite 혼합 컬럼에서 환원 구역 형성과 Cr(VI) 제거
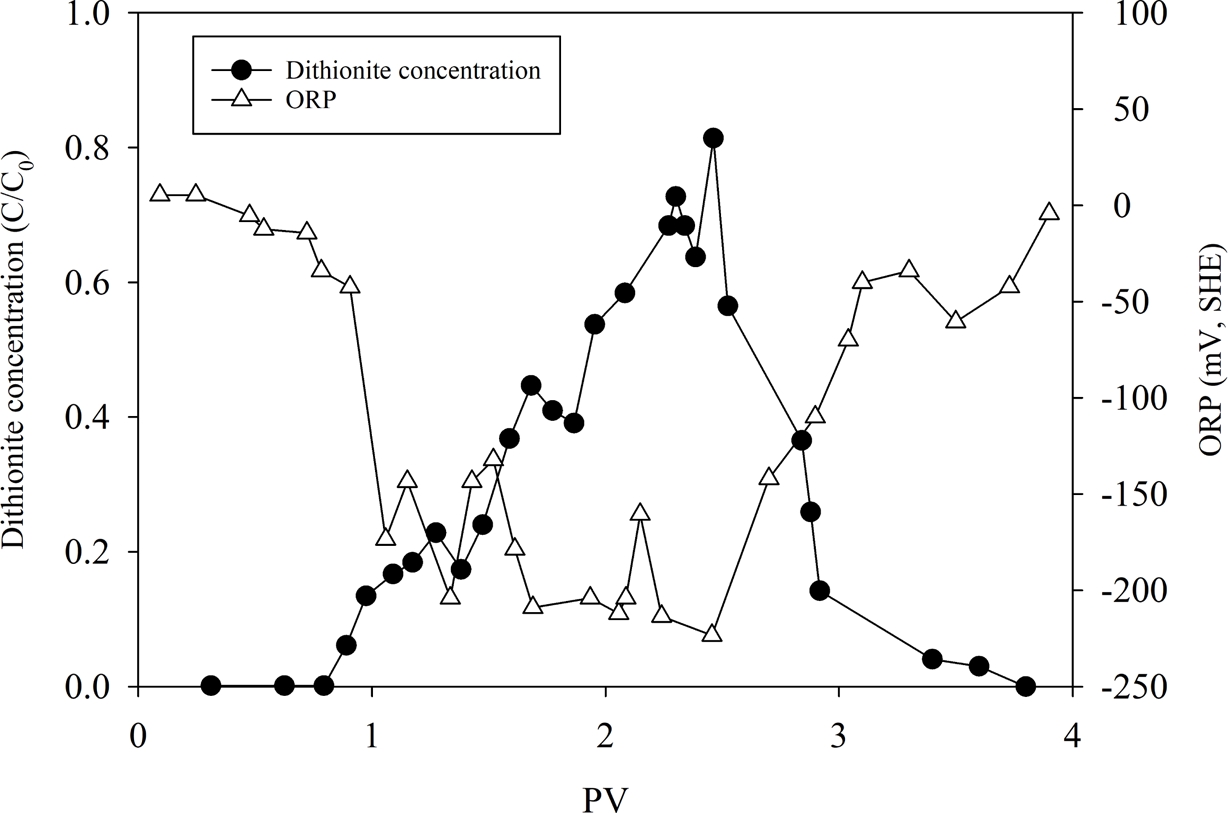
Fig. 5는 50 mM dithionite를 2 PV 동안 pulse로 주입했을 때의 농도와 ORP 변화를 보여준다. 주입된 dithionite는 컬럼 내부를 따라 이동하면서 점차 소모되었고, ORP는 약 -200 mV(SHE)까지 낮아졌다. 형성된 환원 조건은 약 3 PV 동안 유지되었으며, 배치 실험에서 확인된 환원 거동이 유동 조건에서도 재현될 수 있음을 확인하였다.
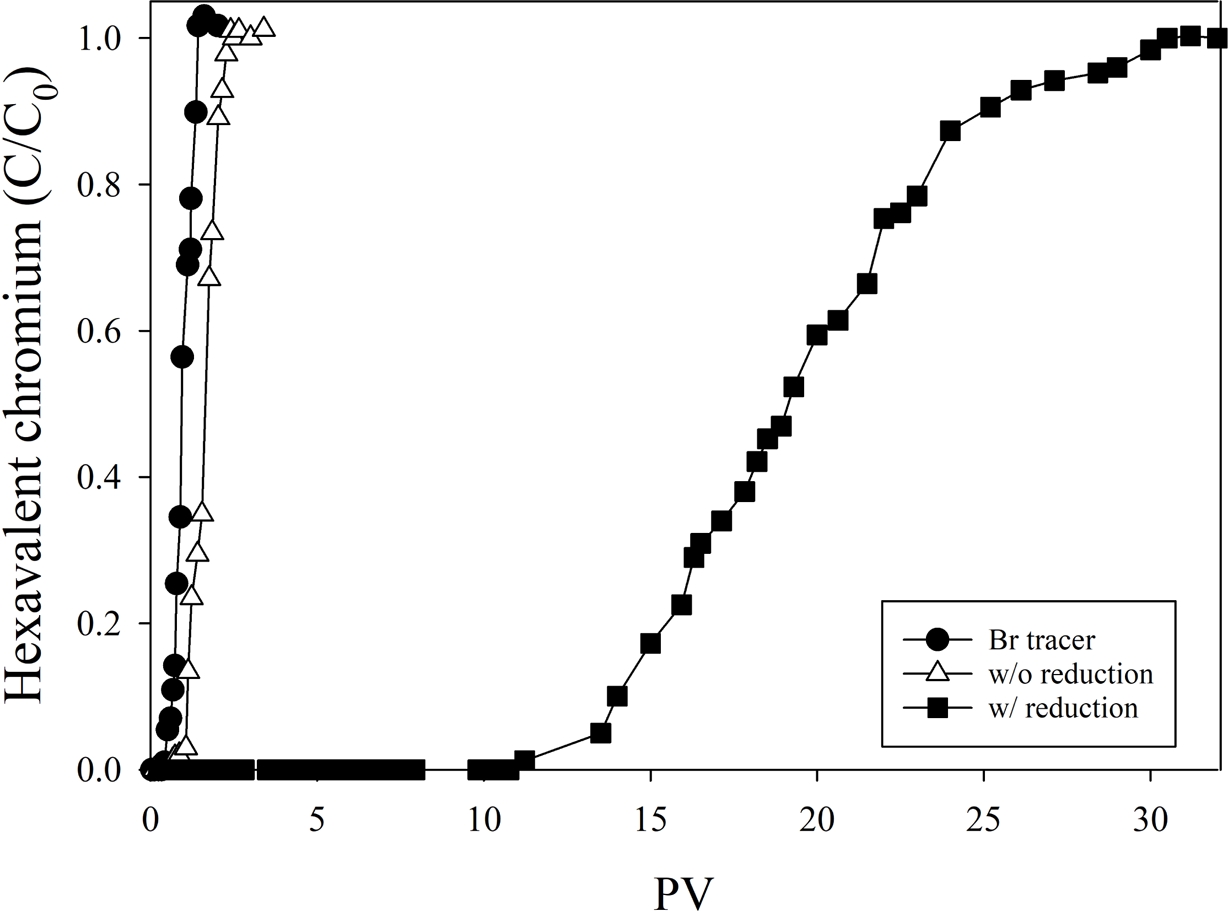
Dithionite 처리 유무에 따라 제조된 컬럼에 50 mg/L Cr(VI) 용액을 지속적으로 주입하여 얻은 각각의 파과곡선을 비교하였다(Fig. 6). 환원 처리를 하지 않은 컬럼에서는 Cr(VI)가 Br⁻ tracer와 유사하게 1 PV 이내에 검출되었고, 이후 곧바로 C/C0가 1에 도달하였다. Cr(VI)가 컬럼 내에서 지연(retardation) 없이 이동한 것은, 배치 실험에서와 마찬가지로 비환원된 montmorillonite 표면에서 흡착이 거의 일어나지 않았던 결과와 일치한다. 반면, dithionite 처리 컬럼에서는 Cr(VI)가 10 PV까지 전혀 검출되지 않았으며, 이후에도 농도가 크게 억제되어 총 제거량이 140 mg에 달하였다. 이러한 거동은 단순한 흡착에 의한 지연으로는 설명할 수 없으며, 컬럼 내에서 Cr(VI)이 Fe(II)에 의해 환원되었음을 시사한다.
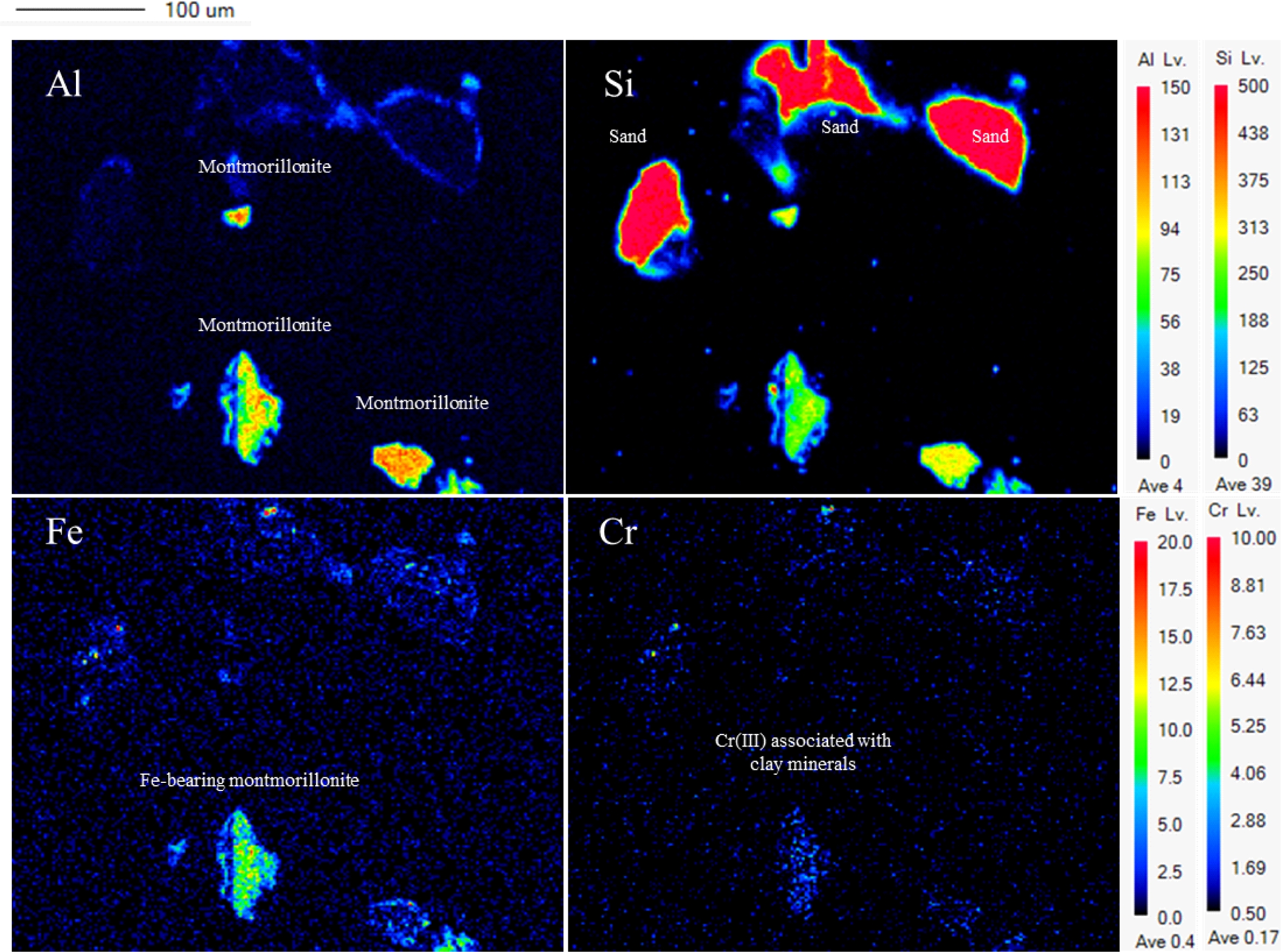
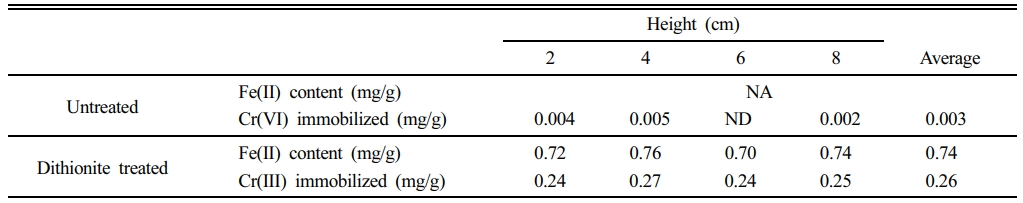
컬럼을 해체하여 단면별 매질 내 구조철과 고정화된 크롬 분석을 수행하였다(Table 2). Dithionite를 주입하지 않은 컬럼에서는 Fe(II) 생성과 Cr(VI) 고정화가 거의 관찰되지 않았다. 반면 dithionite 처리 컬럼에서는 구조철이 배치 실험과 유사하게 약 67% 환원되었으며(Fe(II)/Total Fe = 0.67), 컬럼 내 montmorillonite 함량 5 wt%를 고려하면 평균 0.74 mg/g의 Fe(II)에 해당한다. Cr(VI) 주입 후 고형상에서 검출된 Cr 함량(평균 0.26 mg/g)은 3:1의 화학양론적 비율과 일치하였다. 이는 구조철 Fe(II)에 의한 Cr(VI)의 환원이 즉시 진행되어 용액상으로 용출되지 않고 고체 표면에서 직접 고정화되었음을 시사한다. EPMA 원소 매핑(Fig. 7)에서도 Cr 신호가 모래 입자가 아닌 Al-Fe이 집중된 montmorillonite 영역에 국한되어 분포하는 것이 확인되어, 환원된 Cr(III)가 점토 표면에 침전된 형태로 고정화되었음을 뒷받침하였다.
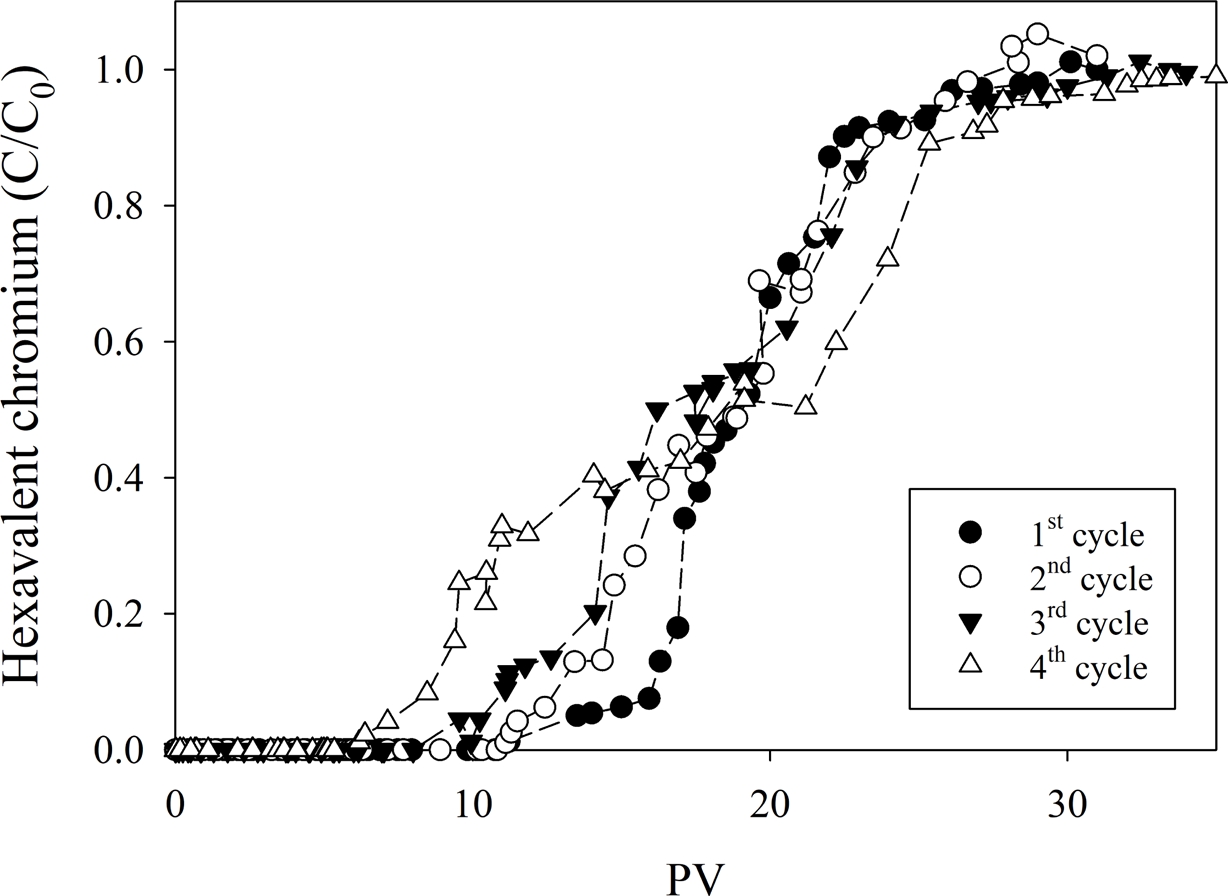
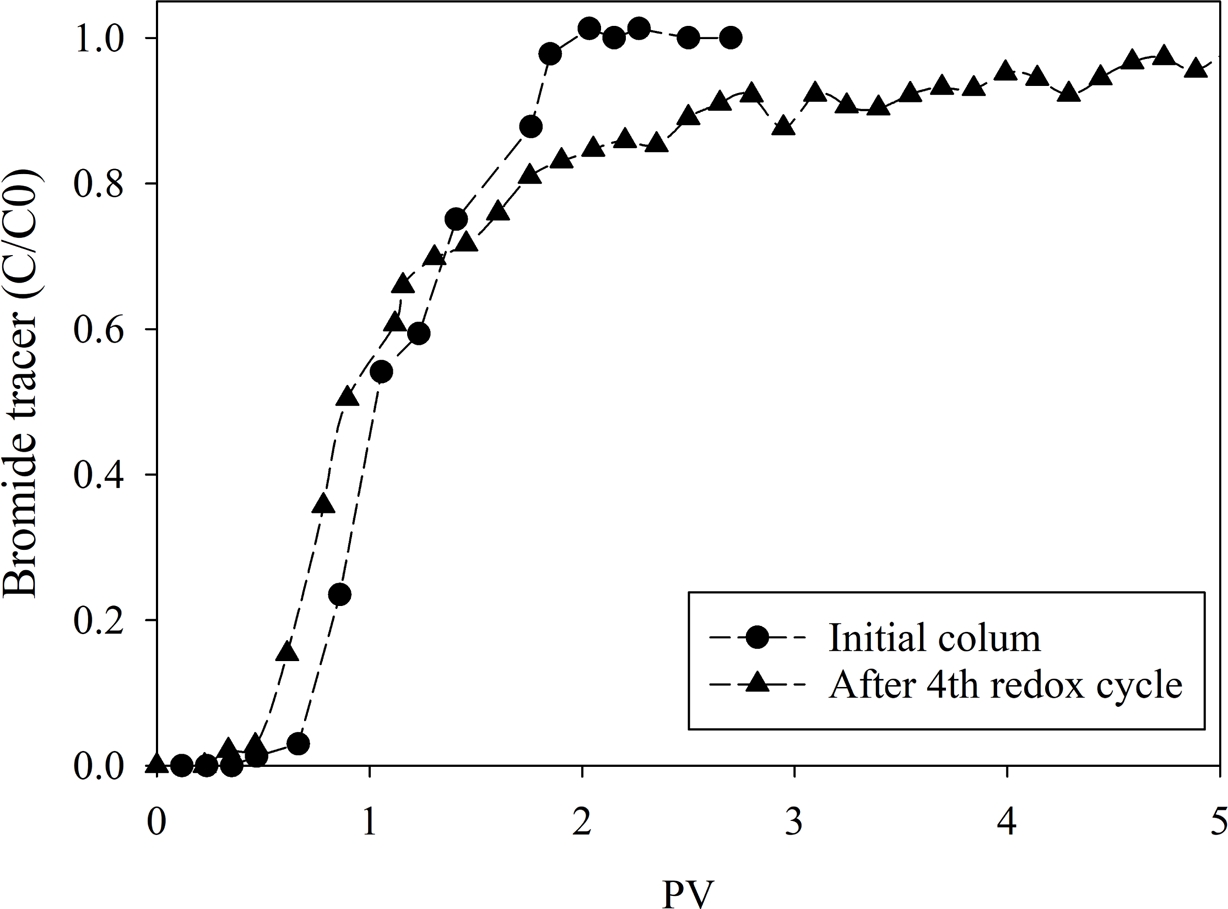
Cr(VI) 제거실험 완료 후 dithionite를 재주입하여 환원 구역의 재생 가능성을 확인하였다. Fig. 8과 같이 dithionite 재주입 시 컬럼 내 Fe(II)가 재형성되며 환원 구역이 복원되고 Cr(VI) 제거 성능이 회복되었다. 4회 재주입을 반복하는 동안 Cr(VI) 파과곡선이 점차 변화하며 사이클이 증가할수록 제거 성능이 다소 감소하는 경향이 나타났으나, 각 사이클에서 여전히 상당한 수준의 Cr(VI) 제거가 유지되었다. 각 사이클별 Fe(II) 용출량과 총 Cr 제거량을 Table 3에 제시하였으며, 재생이 반복될수록 구조철 용출량이 증가하여 Cr(VI)의 제거량 감소가 확인되었다. 또한 1차 및 4차 사이클 종료 후 Br⁻ tracer test(Fig. 9)에서 조기 파과 및 tailing 증가가 관찰되었는데, 이는 점토 입자 응집이나 Cr(III) 침전물로 인한 pore clogging에 의해 우선흐름(preferential flow)가 일부 형성된 것으로 해석된다.
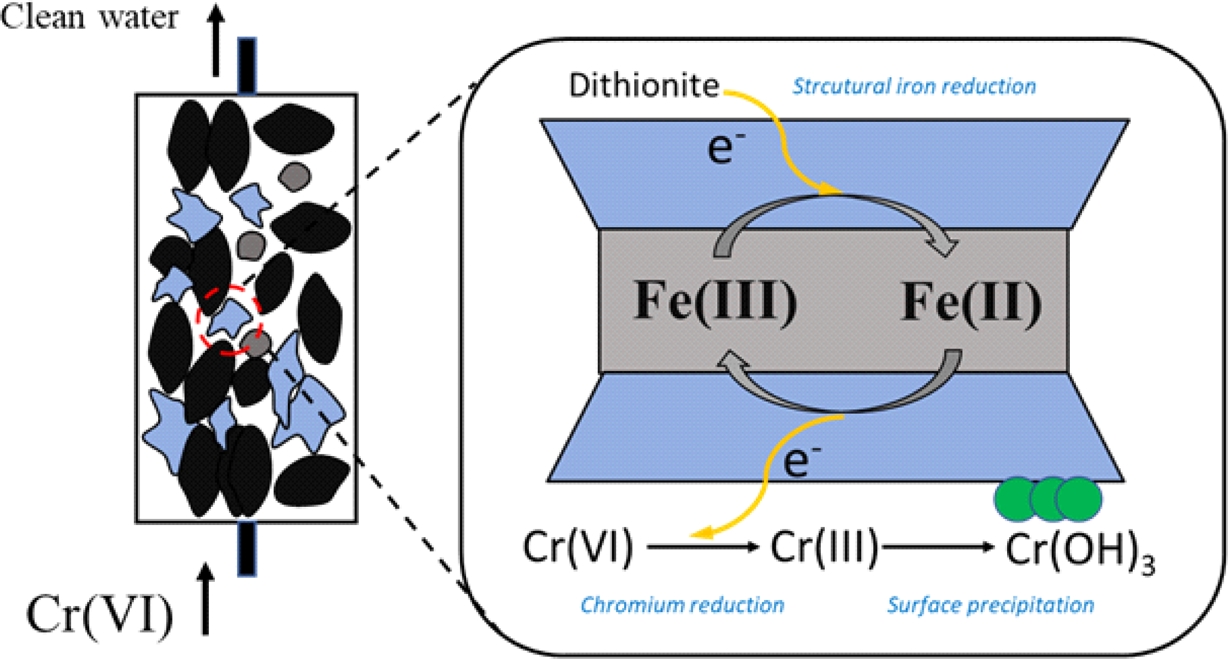
그럼에도 불구하고, 본 연구의 결과는 dithionite 재주입이 환원 구역의 수명을 연장하고 장기적인 Cr(VI) 제거 효과를 유지하는 유효한 수단이 될 수 있음을 보여준다. 이상의 결과를 바탕으로, 본 연구에서 제안한 환원 구역 내 전자전달 및 Cr(VI) 고정화 과정을 개념적으로 나타낸 모식도를 Fig. 10에 제시하였다.
|
Fig. 1 (a) Structural Fe(II) content of montmorillonite with increasing dithionite concentration, (b) Linear relationship between Fe(II)/Fe(III) ratio and redox potential. |
|
Fig. 2 Comparison of Cr(VI) and total Cr removal efficiency between reduced (Fe(II)-bearing) and non-treated montmorillonite. |
|
Fig. 3 Cr(VI) removal capacity and Fe(II) consumption by solid to liquid ratio. |
|
Fig. 4 Characterization of Cr reduction products associated with montmorillonite; (a) SEM image of montmorillonite surface, (b) EDS mapping showing Cr precipitates on the clay surface, (c) XPS spectra of Cr 2p confirming the presence of Cr(III). |
|
Fig. 5 Dithionite concentration and ORP of effluent after pulse injection of dithionite in the column. |
|
Fig. 6 Breakthrough curves of Cr(VI) in columns with and without dithionite reduction, compared with Br tracer. |
|
Fig. 7 EPMA elemental mapping of column materials showing Cr(III) associated with Fe-bearing montmorillonite. |
|
Fig. 8 Cr(VI) breakthrough curves during four successive dithionite reinjection cycles showing regeneration behavior. |
|
Fig. 9 Br⁻ tracer breakthrough curves after the 1st and 4th regeneration cycles. |
|
Fig. 10 Conceptual illustration of the reductive zone formation and Cr(VI) immobilization mechanism mediated by structural Fe(II) in clay minerals. |
|
Table 1 Fe(II) regeneration and Cr(VI) reduction performance through repetitive dithionite treatment cycles |
|
Table 2 Depth profiles of Fe(II) content and immobilized Cr in untreated and dithionite-treated columns |
|
Table 3 Changes in structural Fe(II) content and Cr(VI) removal capacity over repeated regeneration cycles |
본 연구에서는 dithionite 주입을 통해 점토광물 내 구조철을 환원시켜 Fe(II)-bearing 광물을 형성하고, 이를 활용한 Cr(VI) 환원 및 고정화를 평가하였다. 배치 실험에서는 dithionite 농도가 증가할수록 Fe(II) 생성량이 증가하였으며, 환원 거동은 산화환원 평형 관계를 따르는 것으로 확인되었다. 환원된 구조철(Fe(II))은 Cr(VI)을 효과적으로 환원시켰으며, 생성된 Cr(III)는 Cr(OH)3의 형태로 침전되어 고정화되었다. 컬럼 실험에서는 dithionite 주입만으로 환원 구역이 형성되었으며, 생성된 환원 구역 내에서 Cr(VI) 파과가 현저히 지연되고 Cr(III)가 montmorillonite와 결합하여 고정화되었다. 또한 dithionite 재주입 시 환원 구역이 재생되면서 Cr(VI) 제거 성능이 회복되었다. 본 연구의 결과는 Fe-bearing 점토광물이 ISRM 기술의 반응 매질로 활용될 수 있는 가능성을 보여주며, 본 연구에서 규명한 dithionite-mediated 구조철 환원 및 전자전달 메커니즘은 U(VI), Se(VI), NO3⁻ 등 다양한 환원민감성 오염물질 제거 기술 개발에 적용될 수 있을 것으로 기대된다. 다만, 본 연구는 균질한 실험실 조건에서 수행되었으므로, 현장 규모로의 확장을 위해서는 다음과 같은 추가 연구가 필요하다. 먼저, 본 기술의 환원 구역 성능 및 수명을 예측하기 위해서는 지하수 유속, 매질 접촉시간, 점토광물 함량 등의 영향을 평가해야 하며, 특히 지하수 내 NO3⁻, Mn(IV), 용존산소 등 electron scavenger들이 Fe(II)를 우선적으로 소모하여 Cr(VI) 제거 효율을 저하시킬 수 있으므로, 다양한 지화학 조건에서 이러한 경쟁 반응의 영향을 정량적으로 규명할 필요가 있다. 또한 본 연구에서 관찰된 재생 사이클별 성능 저하(구조철 용출, 우선흐름)를 고려할 때, 최적 재주입 주기 및 환원 구역의 최대 재생 가능 횟수를 결정하기 위한 장기 모니터링 연구가 필요하다. 아울러 대수층의 불균질성(투수성 분포, 점토 함량 변이 등)이 dithionite 확산 범위 및 환원 구역 형성에 미치는 영향을 평가하기 위해서는 pilot-scale 현장 실증이 선행되어야 할 것이다.
본 연구는 과학기술정보통신부의 재원으로 한국연구재단 연구개발사업의 지원(NRF-2022R1A2C1092732)과 환경부의 재원으로 한국환경산업기술원의 지중환경오염·위해관리기술개발사업의 지원(RS-2018-KE000140)을 받아 수행되었습니다. 또한 서울대학교 공학연구원의 기술적 지원에 감사드립니다.
- 1. Amonette, J.E. and Templeton, J.C., 1998. Improvements to the quantitative assay of nonrefractory minerals for Fe (II) and total Fe using 1, 10-phenanthroline. Clays and Clay Minerals, 46(1), 51-62. https://doi.org/10.1346/CCMN.1998.0460106
-

- 2. Biesinger, M.C., Payne, B.P., Grosvenor, A.P., Lau, L.W.M., Gerson, A.R., and Smart, R.S.C., 2004, Resolving surface chemical states in XPS analysis of first row transition metals, oxides and hydroxides: Cr, Mn, Fe, Co and Ni. Applied Surface Science, 257(7), 2717-2730. https://doi.org/10.1016/j.apsusc.2010.10.051
-

- 3. Boparai, H.K., Comfort, S., Shea, P.J., and Szecsody, J.E., 2008, Remediating explosive-contaminated groundwater by in situ redox manipulation (ISRM) of aquifer sediments. Chemosphere, 71(5), 933-941, https://doi.org/10.1016/j.chemosphere.2007.11.001
-

- 4. Buerge, I.J. and Hug, S.J., 1997, Kinetics and pH dependence of chromium (VI) reduction by iron (II). Environmental Science & Technology, 31(5), 1426-1432. https://doi.org/10.1021/es960672i
-

- 5. DesMarias, T.L. and Costa, M., 2019, Mechanisms of chromium-induced toxicity. Current Opinion in Toxicology, 14, 1-7. https://doi.org/10.1016/j.cotox.2019.05.003
-

- 6. Du, J., Bao, J., Lu, C., and Werner, D., 2016, Reductive sequestration of chromate by hierarchical FeS@Fe0 particles. Water Research, 102, 73-81. https://doi.org/10.1016/j.watres.2016.06.009
-

- 7. Fruchter, J.S., Amonette, J.E., and Cole, C.R., 1996, In Situ Redox Manipulation Field Injection Test Report-Hanford 100-H Area (No. PNNL--11372). Pacific Northwest National Lab., Richland, WA (United States).
-

- 8. Gorski, C.A., Klüpfel, L.E., Voegelin, A., Sander, M., and Hofstetter, T.B., 2013, Redox properties of structural Fe in clay minerals: 3. Relationships between smectite redox and structural properties. Environmental Science & Technology, 47(23), 13477-13485. https://doi.org/10.1021/es403824x
-

- 9. Guerra, D.J.L., Mello, I. Freitas, L.R., Resende, R.A.R., and Silva, R.A.R., 2014. Equilibrium, thermodynamic, and kinetic of Cr(VI) adsorption using a modified and unmodified bentonite clay. International Journal of Mining Science and Technology, 24(4), 525‑535. https://doi.org/10.1016/j.ijmst.2014.05.017
-

- 10. Guo, H., Liu, C., Yan, S., Yin, J., and Shan, J., 2024, Source, distribution, and geochemical processes of geogenic high chromium groundwater around the world: A critical review. Journal of Hydrology, 638, 131480. https://doi.org/10.1016/j.jhydrol. 2024.131480
-

- 11. He, Y.T. and Traina, S.J., 2005, Cr (VI) reduction and immobilization by magnetite under alkaline pH conditions: the role of passivation. Environmental Science & Technology, 39(12), 4499-4504. https://doi.org/10.1021/es0483692
-

- 12. Ilgen, A.G., Kukkadapu, R.K., Leung, K., and Washington, R.E., 2019, ¡°Switching on¡± iron in clay minerals. Environmental Science: Nano, 6(6), 1704-1715. https://doi.org/10.1039/C9EN00228F
-

- 13. Istok, J.D., Amonette, J.E., Cole, C.R., Fruchter, J.S., Humphrey, M.D., Szecsody, J.E., Teel, S.S., Vermeul, V.R., Williams, M.D., and Yabusaki, S.B., 1999, In situ redox manipulation by dithionite injection: Intermediate-scale laboratory experiments. Groundwater, 37(6), 884-889. https://doi.org/10.1111/j.1745-6584.1999. tb01187.x
-

- 14. Joe-Wong, C., Brown Jr, G.E., and Maher, K., 2017, Kinetics and products of chromium (VI) reduction by iron (II/III)-bearing clay minerals. Environmental Science & Technology, 51(17), 9817-9825. https://doi.org/10.1021/acs.est.7b02934
-

- 15. Komadel, P., Madejová, J., and Stucki, J.W., 2006, Structural Fe (III) reduction in smectites. Applied Clay Science, 34(1-4), 88-94. https://doi.org/10.1016/j.clay.2005.10.016
-

- 16. Moon, C., Kim, B. C., and Nam, K., 2025, Redox behavior of structural iron by dithionite in Fe (¥²)-bearing clay minerals and its utilization as an electron shuttle for redox-sensitive contaminants. Journal of Environmental Chemical Engineering, 117250. https://doi.org/10.1016/j.jece.2025.117250
-

- 17. Mullet, M., Boursiquot, S., and Ehrhardt, J.J., 2004, Removal of hexavalent chromium from solutions by mackinawite, tetragonal FeS. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 244(1-3), 77-85. https://doi.org/10.1016/j.colsurfa. 2004.06.013
-

- 18. Neumann, A., Sander, M., and Hofstetter, T.B., 2011, Redox properties of structural Fe in smectite clay minerals. In P. Tratnyek, T.B. Hofstetter, & S.M. Bornick (Eds.), Aquatic Redox Chemistry (pp. 361-379). ACS Publications. https://doi.org/10.1021/bk-2011-1071.ch017
-

- 19. Ribeta, I., Ptacek, C.J., Blowes, D.W., and Jambor, J.L., 1995, The potential for metal release by reductive dissolution of weathered mine tailings. Journal of Contaminant Hydrology, 17(3), 239-273. https://doi.org/10.1016/0169-7722(94)00010-F
-

- 20. Richard, F.C. and Bourg, A.C.M., 1991, Aqueous geochemistry of chromium: A review. Water Research, 25(7), 807-816. https://doi.org/10.1016/0043-1354(91)90160-R
-

- 21. Stucki, J.W., Lee, K., Zhang, L., Larson, R.A., and Traina, S.J., 1996, Effects of reduction and reoxidation of structural Fe on the surface chemistry of smectite. Clays and Clay Minerals, 44(3), 450-454. https://doi.org/10.1346/CCMN.1984.0320502
- 22. Tsarev, S., Waite, T.D., and Collins, R.N., 2016, Uranium reduction by Fe (II) in the presence of montmorillonite and nontronite. Environmental Science & Technology, 50(15), 8223-8230. https://doi.org/10.1021/acs.est.6b02000
-

- 23. Vermeul, V.R., Williams, M.D., Szecsody, J.E., Fruchter, J.S., Cole, C.R., and Amonette, J.E., 2003, Creation of a subsurface permeable reactive barrier using in situ redox manipulation. In Handbook of Groundwater Remediation using Permeable Reactive Barriers (pp. 163-192). Academic Press. https://doi.org/10.1016/B978-012513563-4/50010-4
-

- 24. Williams, A.G. and Scherer, M.M., 2001, Kinetics of Cr (VI) reduction by carbonate green rust. Environmental Science & Technology, 35(17), 3488-3494. https://doi.org/10.1021/es010579g
-

- 25. Yu, C., Qian, A., Lu, Y., Liao, W., Zhang, P., Tong, M., Dong, H., Zeng, Q., and Yuan, S., 2024, Electron transfer processes associated with structural Fe in clay minerals. Critical Reviews in Environmental Science and Technology, 54(1), 13-38. https://doi.org/10.1080/10643389.2023.2221154
-

- 26. Zulfiqar, U., Haider, F.U., Ahmad, M., Hussain, S., Maqsood, M.F., Ishfaq, M., Shahzad, B., Waqas, M.M., Ali, B., Tayyab, M.N., Ahmad, S.A., Khan, I., and Eldin, S.M., 2023, Chromium toxicity, speciation, and remediation strategies in soil-plant interface: A critical review. Frontiers in Plant Science, 13, 1081624. https://doi.org/10.3389/fpls.2022.1081624
-

 This Article
This Article
-
2025; 30(6): 63-72
Published on Dec 31, 2025
- 10.7857/JSGE.2025.30.6.063
- Received on Oct 10, 2025
- Revised on Oct 21, 2025
- Accepted on Nov 9, 2025
 Services
Services
Shared
 Correspondence to
Correspondence to
- Kyoungphile Nam
-
Department of Civil and Environmental Engineering, Seoul National University, Seoul 08826, South Korea
- E-mail: kpnam@snu.ac.kr





